
Kohlenstoffdisulfid
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK |
| ||||||||
| Toxikologische Daten | 1200 mg/kg (LD50, Ratte, oral) | ||||||||
Kohlenstoffdisulfid (Trivialname: Schwefelkohlenstoff, CS2) ist ein Sulfid des Kohlenstoffs.
Geschichte
Kohlenstoffdisulfid wurde 1796 von Wilhelm August Lampadius entdeckt. Im letzten Viertel des 19. Jahrhunderts gab es mehrere erfolglose Versuche, Kohlenstoffdisulfid als Arbeitsflüssigkeit für Dampfmaschinen einzusetzen. Schwefelkohlenstoff wurde auf Grund seiner hohen Toxizität auch zur Vernichtung von Ratten und Wühlmäusen eingesetzt. Die toxische Wirkung wurde 1866 beschrieben.
Wegen seiner guten Lösungsmitteleigenschaften wurde Schwefelkohlenstoff z.B. als Lösemittel für weißen Phosphor in Phosphorbomben oder bei der Vulkanisation von Kautschuk nach dem Kaltvulkanisationsverfahren verwendet. Dieses Verfahren wurde jedoch durch die Heißvulkanisation verdrängt.

Die Bodeninjektion mit Schwefelkohlenstoff war eine wirksame, arbeitsaufwändige und teure Methode zur Bekämpfung der Reblaus. Man brachte den flüssigen, leicht verdunstenden, giftigen Schwefelkohlenstoff mit Handinjektoren in den Hauptwurzelbereich von befallenen Rebstöcken. Durch die Veredlung der Edelsorte mit einer widerstandsfähigen Unterlagsrebe wurde diese Möglichkeit überflüssig und ist seit 1997 verboten.
Gewinnung und Darstellung
Kohlenstoffdisulfid besitzt eine positive Standardbildungsenthalpie (für flüssiges CS2: ΔHf = +89,7 kJ/mol), die Synthese aus den Elementen ist damit eine endotherme Reaktion. Beim Zerfall in die Elemente Schwefel und Kohlenstoff kann die Verbindung den entsprechenden Energiebetrag wieder abgeben. Der Zerfall erfolgt jedoch nicht spontan, da es sich um eine metastabile Verbindung handelt.
Die Synthese aus den Elementen erfolgte bis in die 1950er Jahre unter Luftausschluss durch Überleitung von Schwefeldämpfen über glühende Holzkohle bei 800–1000 °C.
Heutzutage wird Kohlenstoffdisulfid aus meist ungereinigtem Erdgas (oder anderen Quellen für Alkane wie z.B. Methan) und Schwefel bei 600 °C in Gegenwart von Katalysatoren synthetisiert. Bei dieser Reaktion entsteht außerdem Schwefelwasserstoff, der industriell weiterverarbeitet wird.
Oftmals entsteht Schwefelkohlenstoff auch auf natürliche Art und Weise, zum Beispiel bei Fäulnisprozessen oder bei geologischen Prozessen. Global gesehen hat Kohlenstoffdisulfid jedoch nur einen geringen Anteil an der gesamten Schwefelemission in die Atmosphäre.
| Strukturformel | |
|---|---|
| Allgemeines | |
| Name | Kohlenstoffdisulfid |
| Andere Namen |
|
| Summenformel | CS2 |
| CAS-Nummer | 75-15-0 |
| PubChem | 6348 |
| ECHA-InfoCard | 100.000.767 |
| Kurzbeschreibung |
farblose, stark lichtbrechende Flüssigkeit, die im Reinzustand angenehm aromatisch, auf Grund von Verunreinigung jedoch meist unangenehm riecht |
| Eigenschaften | |
| Molare Masse | 76,14 g/mol |
| Aggregatzustand | flüssig |
| Dichte | 1,26 g/cm3 |
| Schmelzpunkt | −112 °C |
| Siedepunkt | 46 °C |
| Dampfdruck |
|
| Löslichkeit |
|
| Brechungsindex | 1,6319 (20 °C) |
| Thermodynamische Eigenschaften | |
| ΔHf0 | 89,0 kJ/mol |
Eigenschaften
Kohlenstoffdisulfid ist eine farblose, stark lichtbrechende Flüssigkeit. In reinem Zustand riecht Schwefelkohlenstoff angenehm wie Ether; durch Verunreinigungen ist dieser etherische Geruch meist nicht mehr wahrnehmbar. Meist sind geringe Mengen von Schwefelverbindungen die Ursache für einen teilweise widerlichen Geruch.
CS2 verbrennt mit einer sehr niedrigen Temperatur (Flammentemperatur unter 200 °C).
Die Verbindung ist ein gutes Lösungsmittel unter anderem für Iod, Schwefel, Selen, weißen Phosphor, Fette, Kautschuk und Harze. Außerdem ist es ein ausgezeichnetes Dielektrikum (Dielektrizitätskonstante εr = 2,632).
Das Kohlenstoffdisulfid-Molekül ist wie Kohlendioxid ein lineares Molekül mit einem sp-hybridisierten C-Atom und zwei (p-p)π-Bindungen.
Sicherheitstechnische Kenngrößen
Kohlenstoffdisulfid bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt unterhalb von −20 °C. Der Explosionsbereich liegt zwischen 0,6 Vol.‑% (19 g/m3) als untere Explosionsgrenze (UEG) und 60,0 Vol.‑% (1900 g/m3) als obere Explosionsgrenze (OEG). Der maximale Explosionsdruck beträgt 8,7 bar und die Sauerstoffgrenzkonzentration 4,6 Vol.‑%. Die Grenzspaltweite wurde mit 0,37 mm bestimmt. Es resultiert damit eine Zuordnung in die Explosionsgruppe IIC. Mit einer Mindestzündenergie von 0,009 mJ sind Dampf-Luft-Gemische extrem zündfähig. Die Zündtemperatur beträgt 95 °C. Der Stoff fällt somit in die Temperaturklasse T6 und ist der einzige Vertreter in dieser Temperaturklasse.
Toxikologie
Da Schwefelkohlenstoff gut fettlöslich ist, wird es über Lunge und Haut leicht aufgenommen. Eine längere Exposition führt zu Vergiftungserscheinungen: Die akute Schwefelkohlenstoffvergiftung äußert sich in Gesichtsrötung, euphorischen Erregungszuständen, dann Bewusstlosigkeit, Koma und Atemlähmung; die chronische Schwefelkohlenstoffvergiftung durch wiederholtes längeres Einatmen äußert sich in Kopfschmerzen, Schlaflosigkeit, Gedächtnis-, Seh- und Hörstörungen, Nervenentzündungen und Gefäßschäden.
Verwendung und Reaktionen
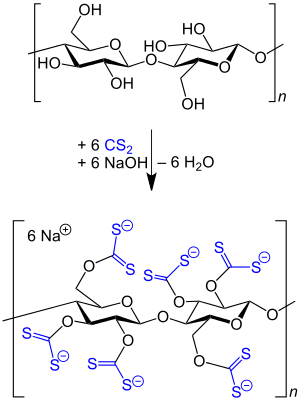
Schwefelkohlenstoff wird in großen Mengen zur Herstellung von Cellulosefasern aus Zellstoff eingesetzt, wobei der Zellstoff zuerst mit Natronlauge zu Alkalicellulose umgesetzt und diese nach dem oxidativen Abbau mit Schwefelkohlenstoff zu dem in Natronlauge löslichen Xanthogenat verarbeitet wird. Die so entstandene Celluloselösung, auch Viskose genannt, wird in schwefelsauren Spinnbädern zu Regeneratcellulose versponnen.
Schwefelkohlenstoff ist ein Lösungsmittel für Fette, Harze, Gummi und Kautschuk. Es wird in der Infrarot-Spektroskopie eingesetzt, da es keine störende Wasserstoff- oder Halogenbanden hat. Außerdem zeigt Schwefelkohlenstoff einen starken Kerr-Effekt und wird daher als Kerrlinse in Festkörperlasern eingesetzt.
Kupferxanthogenate setzen unter Zersetzung giftigen Schwefelkohlenstoff frei, was früher zur Schädlingsbekämpfung eingesetzt wurde.
Die Reduktion mit Natrium in Dimethylformamid ergibt das Dinatriumsalz von DMIT, Kurzbezeichnung für Dimercaptoisotrithion, einer Ausgangsverbindung zur Herstellung schwefelreicher Heterocyclen und von substituierten Tetrathiafulvalenen.
Beim Kochen mit wässrigen Sulfid-Lösungen entstehen Trithiocarbonate. Bei der Reaktion mit Grignard-Verbindungen entstehen durch eine Insertionsreaktion Magnesiumsalze, deren Hydrolyse Dithiocarbonsäuren (R–CSSH) ergibt. Mit Ammoniak, primären und sekundären Aminen entstehen Dithiocarbamate.
Spuren von Schwefelkohlenstoff (ca. 1 mg/l) werden dem Elektrolytbad bei der galvanischen Silberabscheidung als Glanzbildner hinzugegeben. Es verursacht einen sofortigen, vorübergehenden Abfall der kathodischen Polarisation. Dadurch ist es möglich, nahezu spiegelglänzende Silberschichten abzuscheiden. Diese Wirkung als sogenannter Glanzbildner ist bereits seit Mitte des 19. Jahrhunderts bekannt.
Kohlenstoffdisulfid hat den gleichen Brechungsindex wie Glas, daher ist in Kohlenstoffdisulfid eingetauchtes Glas praktisch unsichtbar. Dies wird beispielsweise zum Erkennen von gefälschten Diamanten verwendet. Echte Diamanten bleiben, anders als Glas, auch beim Eintauchen gut sichtbar. Es kann auch zur Synthese von künstlichen Diamanten eingesetzt werden.
Nachweis
Kohlenstoffdisulfid gibt mit Diethylamin in Gegenwart von Kupfersalzen (Cu2+) einen gelben Dithiocarbamat-Komplex:
Andere Nachweisverfahren, wie die Bildung von roten Kristallen durch Reaktion mit Triethylphosphin, sind ebenfalls bekannt.
Messtechnische Erfassung von Kohlenstoffdisulfid in Abgasen und in der Luft
Kohlenstoffdisulfid-Emissionen können mit einem iodometrischen Titrationsverfahren ermittelt werden, bei dem ein Teilstrom des zu beprobenden Abgases zunächst durch eine Cadmiumacetat-Lösung geleitet wird, um etwaigen Schwefelwasserstoff zu absorbieren. Die Bindung des Kohlenstoffdisulfids erfolgt in ethanolischer Kalilauge. Das so gewonnene Kaliumethylxanthogenat wird im Anschluss mit einer eingestellten Iodlösung titriert. Dieses Verfahren wird erfolgreich in der Viskose verarbeitenden Industrie angewendet.
Gängige Verfahren zur Bestimmung von Kohlenstoffdisulfid in der Arbeitsplatzluft basieren auf der Adsorption an Aktivkohle mit anschließender Desorption und gaschromatographischer Analyse des desorbierten Stoffs.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 15.09. 2025


