
Malonsäure
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| Toxikologische Daten | 1310 mg/kg (LD50, Ratte, oral) | |||||||
Malonsäure (Propandisäure) ist eine bei Raumtemperatur kristalline Dicarbonsäure, deren Ester und Salze Malonate genannt werden (z.B. Diethylmalonat = Malonsäurediethylester).
Geschichte und Vorkommen
Malonsäure wurde 1858 bei der Oxidation der Äpfelsäure entdeckt. Der Name leitet sich von lat. malum = Apfel (Pflanzengattung) ab. Malonsäure kommt im Zuckerrübensaft vor. Malonsäure ist ein Zellgift, das durch Hemmung der Succinat-Dehydrogenase den Ablauf des Citratzyklus (Krebszyklus) hemmt.
Darstellung und Gewinnung
Malonsäure wird unter anderem durch Umsetzung von Chloressigsäure mit Natriumcyanid (NaCN) (Kolbe-Nitrilsynthese) und anschließender Hydrolyse der entstandenen Cyanessigsäure hergestellt.
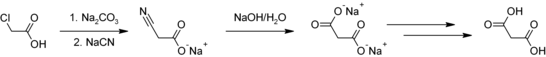
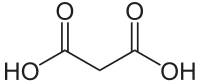
| Strukturformel | ||
|---|---|---|
 | ||
| Allgemeines | ||
| Name | Malonsäure | |
| Andere Namen |
| |
| Summenformel | C3H4O4 | |
| Kurzbeschreibung | farblose Kristalle | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | 141-82-2 | |
| EG-Nummer | 205-503-0 | |
| ECHA-InfoCard | 100.005.003 | |
| PubChem | 867 | |
| ChemSpider | 844 | |
| DrugBank | DB02175 | |
| Eigenschaften | ||
| Molare Masse | 104,06 g/mol | |
| Aggregatzustand | fest | |
| Dichte | 1,60 g/cm3 | |
| Schmelzpunkt | 132–135 °C | |
| Siedepunkt | Zersetzung ab 140 °C | |
| Dampfdruck | 0,1 Pa (18,5 °C) | |
| pKS-Wert |
| |
| Löslichkeit |
| |
Eigenschaften
Malonsäure bildet farb- und geruchlose Kristalle, die einen Schmelzpunkt von 136 °C besitzen und sich in Wasser leicht lösen. Die Verbindung tritt in drei polymorphen Kristallformen auf. Eine γ–Form existiert nur bei tiefen Temperaturen und wandelt sich bei −225,9 °C in die β–Form um. Die Phasenumwandlung von der β–Form zur α–Form erfolgt bei 79 °C. Die Formen α und β bzw. β und γ stehen enantiotrop zueinander. Der Feststoff zersetzt sich oberhalb des Schmelzpunktes unter Kohlenstoffdioxidabspaltung zu Essigsäure. In wässriger Lösung findet diese Decarboxylierung ab 70 °C statt. In höher siedenden Lösungsmitteln, wie Ethylenglycol, Trimethylenglycol, 1,3-Butandiol und 2,3-Butandiol verläuft die Reaktion oberhalb von 100 °C als Reaktion erster Ordnung.
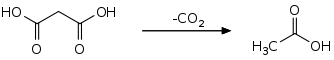
Erhitzt man Malonsäure mit stark wasserentziehenden Mitteln, z.B. mit Phosphorpentoxid, so entsteht durch intramolekulare Wasserabspaltung in schlechter Ausbeute Kohlenstoffsuboxid, auch Malonsäureanhydrid genannt.
Malonsäure ist eine CH-acide Verbindung, d.h., durch den elektronenziehenden Effekt der beiden Carboxygruppen kann am zentralen Kohlenstoff leicht ein Proton abgespalten werden.
Verwendung
Malonsäurederivate sind Synthesebausteine bei der Knoevenagel-Kondensation oder der Malonestersynthese und dienen beispielsweise zur Herstellung von Barbitursäure und deren Derivaten. Insbesondere gelang William Henry Perkin, jr. erstmals eine Cyclopropanierung durch Umsetzung des C-H-aciden Malonsäurediethylesters mit 1,2-Dibromethan und zwei Äquivalenten Natriumethanolat. Beim Erhitzen von Gemischen cyclischer Imine mit Malonsäure entstehen β-Aminocarbonsäuren. Es werden jährlich 10 bis 100 Tonnen nach Europa importiert.
Malonat: Verwechslungsgefahr mit Malat und Maleat
Malonat darf nicht mit dem Säureanion der Äpfelsäure, dem Malat-Ion, oder dem Anion der Maleinsäure, dem Maleat verwechselt werden.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 27.03. 2026

