Propen
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| MAK | Schweiz: 10000 ml/m3 bzw. 17500 mg/m3 | |||||||
Propen [proˈpeːn] (Propylen [propyˈleːn]) ist ein farbloses brennbares Gas. Es wird durch thermische Spaltung (Steamcracken) der bei der Erdölverarbeitung anfallenden Leichtbenzine erhalten.
| Strukturformel | |
|---|---|
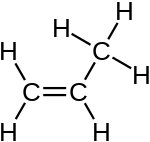
| |
| Allgemeines | |
| Name | Propen |
| Andere Namen |
|
| Summenformel | C3H6 |
| Kurzbeschreibung | farbloses, geruchloses Gas |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 115-07-1 |
| EG-Nummer | 204-062-1 |
| ECHA-InfoCard | 100.003.693 |
| PubChem | 8252 |
| Eigenschaften | |
| Molare Masse | 42,08 g/mol−1 |
| Aggregatzustand | gasförmig |
| Dichte |
1,91 kg/m3 (0 °C, 1013 hPa) 0,609 kg/l1 am Siedepunkt |
| Schmelzpunkt | −185,3 °C |
| Siedepunkt | −47,7 °C |
| Dampfdruck |
|
| Löslichkeit | schwach löslich in Wasser (384 mg/l, 20 °C, 0,1 MPa) |
| Dipolmoment | 0,366 D (1,22 · 10−30 C · m) |
| Brechungsindex | 1,3567 (−70 °C) |
| Thermodynamische Eigenschaften | |
| ΔHf0 | 20,0 kJ/mol |
Herstellung
Propen wird vorwiegend durch Steamcracken von längerkettigen Alkanen (C5-C10) synthetisiert:
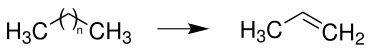
Propan-Dehydrierung (PDH)
Alternativ kann Propen durch thermisch-katalytische Behandlung von Propan unter Wasserstoffabspaltung dargestellt werden:

Dieses Verfahren wird unter anderem von BASF Sonatrach in Tarragona angewandt.
Der wichtigste Prozess der Propan-Dehydrierung ist der Oleflex-Prozess von UOP, auf dem 55 % der weltweiten Kapazität basiert. Bei ihm wird ein propanhaltiges Gas auf 600–700 °C vorgeheizt und in einem Fließbett-Dehydrierreaktor an einem Platin-Katalysator mit Aluminiumoxid als Träger dehydriert.
Weitere Verfahren
Propen kann außerdem per Olefinmetathese aus Ethylen und Butenen oder durch den Mobil-Prozess aus Methanol (Methanol-to-propylene) gewonnen werden.
Eigenschaften
Chemische Eigenschaften
In Wasser ist Propen nur schwach löslich; das Gas ist brennbar. Aufgrund seiner Doppelbindung ist Propen ein ungesättigter Kohlenwasserstoff und neigt deshalb zu Additionsreaktionen, unter anderem mit Wasserstoff und Halogenen.
Beispiele:
Propen reagiert mit Brom zu 1,2-Dibrompropan:
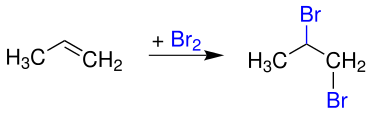
Propen reagiert mit Wasserstoff zu Propan:
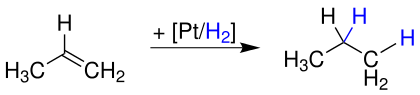
Damit die Additionsreaktion ablaufen kann, werden z. B. Platin-, oder Palladiumkatalysatoren verwendet.
Bei der (säurekatalysierten) Addition von Wasser entsteht 2-Propanol:
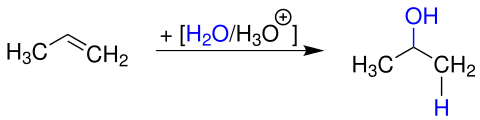
Hexafluorpropen ist die vollständig fluorierte Form des Propens.
Durch Polymerisation von Propen entsteht der weitverbreitete thermoplastische Kunststoff Polypropylen.
Sicherheitstechnische Kenngrößen
Propen bildet mit Luft leicht entzündliche Gemische. Der Explosionsbereich liegt zwischen 1,8 Vol.‑% (32 g/m3) als untere Explosionsgrenze (UEG) und 11,2 Vol.‑% (200 g/m3) als obere Explosionsgrenze (OEG).) Der maximale Explosionsdruck beträgt 9,4 bar. Die Grenzspaltweite wurde mit 0,91 mm bestimmt. Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA. Die Zündtemperatur beträgt 485 °C. Der Stoff fällt somit in die Temperaturklasse T1.
Verwendung
Propen wird als Gas für das Brennschneiden und Ähnliches verwendet und ist ein Kältemittel in industriellen Kälteanlagen (R-1270). Weiterhin ist es einer der wichtigsten Grundstoffe der chemischen Industrie und dient zur Herstellung von Folgeprodukten wie zum Beispiel:
- Aceton
- Acrolein (Propenal)
- Acrylnitril
- Acrylsäure
- Allylverbindungen
- Butanal
- 1-Butanol
- Polypropylen
- Propylenoxid
- 1,2-Propandiol, 1,3-Propandiol
- Thymol
Ungefähr zwei Drittel des Propens werden für die Herstellung von Polypropylen verwendet. Die nächstgrößten Einsatzgebiete sind die Herstellung von Acrylnitril, das vorwiegend für die Fabrikation von Acryl-Textilfasern verwendet wird, und Propylenoxid, als Rohstoff für Produkte wie Polyurethan, Lacke und Klebstoffe, Polyesterharze, Kühl-, Frostschutz- und Lösungsmittel gebraucht werden. Rund 5 Prozent des Propens werden zur Herstellung von Phenol und Aceton im Cumolhydroperoxid-Verfahren eingesetzt.
Sicherheitshinweise
Propen ist wenig giftig, wirkt aber bei hoher Konzentration narkotisierend und erstickend. Da Propen eine größere Dichte als Luft hat und brennbar ist, bilden sich mit Luft leicht explosionsfähige Gemische, indem sich das Propen in Bodennähe ansammelt.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 05.08. 2024

