
Tetrahydrofolsäure
| Sicherheitshinweise | |||
|---|---|---|---|
|
Tetrahydrofolsäure (H4Folat, FH4, THF, hier aber Verwechslungsgefahr zu Tetrahydrofuran), auch Coenzym F, ist ein biochemisches Derivat der Folsäure (Vitamin B9) und fungiert – gebunden an eine Polyglutaminsäure – im Stoffwechsel aller Lebewesen als wichtiger Methylgruppen-Donator.
Biologische Bedeutung
| Strukturformel | ||
|---|---|---|
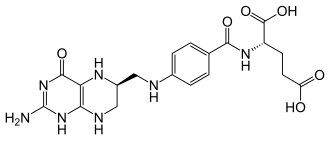
| ||
| Allgemeines | ||
| Name | Tetrahydrofolsäure | |
| Andere Namen |
| |
| Summenformel | C19H23N7O6 | |
| Kurzbeschreibung | gelblicher bis brauner Feststoff[1] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| PubChem | | |
| DrugBank | | |
| Eigenschaften | ||
| Molare Masse | 445,43 g/mol | |
| Aggregatzustand | fest[1] | |
Tetrahydrofolsäure und ihre Derivate sind von besonderer Bedeutung im Aminosäure-, Pyrimidin- und Purin-Stoffwechsel sowie bei der Homoacetatgärung. Sie wird zur Entgiftung von Ameisensäure, die aus Methanol gebildet wird, benötigt.
Biosynthese und Transport
Biosynthetisch entsteht FH4 aus FH2, das selbst aus Folsäure entsteht. Katalysiert werden beide Reaktionen vom Enzym Dihydrofolatreduktase. Stoffe, die dieses Enzym in seiner Funktion hemmen, wie z. B. Methotrexat (Antimetabolit), wirken als Zellgifte.
Wirkungsort von FH4 ist im Zytosol und in den Mitochondrien von Zellen. Um FH4 zunächst vom Blutplasma ins Zytosol zu verschaffen, produziert die Zelle das Transportprotein Folattransporter 1, der die Ein- und Ausschleusung katalysiert. Um ins Innere des Mitochondriums zu gelangen, gibt es gleichermaßen den mitochondrialen Folattransporter.[4]
Reaktionen als Substrat
FH2, FH4 und seine Derivate werden durch Bindung an Polyglutaminsäure (Polyglutamat) an der Ausschleusung gehindert und so im Zytosol und den Mitochondrien der Zellen gespeichert. Nur in dieser Form können viele der kohlenstoffübertragenden Reaktionen stattfinden. Für die Bindung von FH2 und FH4 an Polyglutamat wird das Enzym Folylpolyglutamat-Synthetase benötigt.
Aus FH4-Polyglutamat werden mehrere abgeleitete Stoffe erzeugt, die als Kohlenstoff-Überträger in wichtigen Stoffwechselwegen fungieren. Meist bleibt nach der Reaktion FH4-Polyglutamat übrig, das wiederverwendet wird.
- 10-Formyl-FH4-Polyglutamat ist Reaktionspartner bei der Biosynthese von IMP und Methionin. Es wird aus FH4-Polyglutamat mithilfe des multifunktionellen Enzyms C1-THF-Synthase hergestellt.
- Formyl-FH4-PG wird mithilfe desselben Enzyms in zwei Schritten zu 5,10-Methylen-FH4-Polyglutamat umgesetzt. Dieses nimmt an der Biosynthese von TMP und an der gegenseitigen Umwandlung von Glycin zu Serin teil.
- Letztgenannter Stoff wiederum wird mit der Methylentetrahydrofolat-Reduktase oder mit Ferredoxin zu 5-Methyl-FH4-Polyglutamat umgewandelt, welches Homocystein zu Methionin methyliert und eine Rolle als Methyl-Überträger bei der bakteriellen Methanbildung spielt.[4][5][6]
Einzelnachweise
- ↑ Hochspringen nach: a b Datenblatt
 Tetrahydrofolsäure, ≥65% (when packaged), powder bei Sigma-Aldrich, abgerufen am 23. Juli 2025
(
Tetrahydrofolsäure, ≥65% (when packaged), powder bei Sigma-Aldrich, abgerufen am 23. Juli 2025
(  PDF).
PDF).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Tetrahydrofolsäure (unspez.):
CAS-Nr.: 29347-89-5,
PubChem:
 1129.
1129.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Hochspringen nach: a b
 Metabolism of folate and pterines. Reactome, abgerufen am 23. Juli 2025.
Metabolism of folate and pterines. Reactome, abgerufen am 23. Juli 2025.
- ↑ Methylierung von Corrinoid
 Reaktion – R02289 in der
Kyoto Encyclopedia of Genes and Genomes.
Reaktion – R02289 in der
Kyoto Encyclopedia of Genes and Genomes.
- ↑ A. J. Creighbaum, T. Ticak, S. Shinde, X. Wang, D. J. Ferguson: Examination of the Glycine Betaine-Dependent Methylotrophic Methanogenesis
Pathway: Insights Into Anaerobic Quaternary Amine Methylotrophy. In: Frontiers in Microbiology. Band 10, 2019, S. 2572,
doi:
 10.3389/fmicb.2019.02572,
10.3389/fmicb.2019.02572,
 PMID 31787957,
PMID 31787957,
 PMC 6855144 (freier Volltext).
PMC 6855144 (freier Volltext).


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 08.03. 2026