
Cholin
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
Cholin [çoˈliːn] (von cholé, deutsch ‚Galle‘) ist ein primärer einwertiger Alkohol und eine quartäre Ammoniumverbindung. Kommerziell erhältlich ist zumeist das Cholinchlorid.
| Strukturformel | ||
|---|---|---|
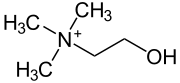
| ||
| Allgemeines | ||
| Name | Cholin | |
| Andere Namen |
| |
| Summenformel |
| |
| Kurzbeschreibung | farbloser, hygroskopischer Feststoff mit schwach aminartigem Geruch | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 200-535-1 | |
| ECHA-InfoCard | ||
| PubChem | ||
| ChemSpider | ||
| DrugBank | ||
| Arzneistoffangaben | ||
| ATC-Code | ||
| Eigenschaften | ||
| Molare Masse | Cholin: 104 g/mol Cholin chlorid: 139,62 g/mol | |
| Aggregatzustand | fest | |
| Schmelzpunkt | Zersetzung bei 180 °C | |
| Löslichkeit |
| |
Geschichte
Cholin wurde im Jahre 1849 von Adolph Strecker in Schweinegalle entdeckt, das Phosphatidylcholin (Lecithin) durch Theodore Gobley 1850. Strecker charakterisierte die Substanz 1862 – er konnte es durch Erhitzen von Lecithin darstellen – und benannte es „Cholin“ nach dem griechischen Wort für Galle. Die 1865 von Oskar Liebreich isolierte Substanz „Neurin“ stellte sich als Cholin heraus, der Name Cholin wurde schließlich akzeptiert. 1866 und 1867 wurde es erstmals chemisch synthetisiert, unabhängig voneinander von Adolf Baeyer und Charles Adolphe Wurtz.
Eugene Kennedy konnte 1954 den Stoffwechselweg identifizieren, bei dem Cholin zu Lecithin umgesetzt wird (CDP-Cholin-Stoffwechselweg). Der Phosphatidylethanolamin-N-methyltransferase (PEMT)-Weg ist ein alternativer Stoffwechselweg zur Bildung von Lecithin aus Cholin, dieser wurde 1960 von Jon Bremer und David Greenberg entdeckt.
Synthese
Cholin kann durch Umsetzung von 2-Chlorethanol mit Trimethylamin hergestellt werden. Andere Synthesen sind die Umsetzung von Trimethylamin mit Ethylenoxid und anschließender Neutralisation mit Salzsäure und die Verseifung von Acetylcholin.
Verwendung
In der Halbleiterproduktion wird Cholin als Reinigungsmittel für Wafer eingesetzt.
In der Biotechnologie findet Cholinchlorid Verwendung in Kulturmedien für Pflanzen.
In Form von 18F-Cholin wird es in der Positronen-Emissions-Tomographie als Tracer bei der Diagnostik des Prostatakarzinoms eingesetzt.
Cholinchlorid ist ein Zusatzstoff in Frackingflüssigkeiten.
Biologische Bedeutung
Vitaminähnliche Substanz
Für den Menschen stellt die Aufnahme von Cholin keine Notwendigkeit dar, solange seine Nahrung die Aminosäure Methionin und Folsäure enthält. Früher galt Cholin als Vitamin und wurde – wie auch das Adenin – als Vitamin B4 bezeichnet, obwohl bekannt war, dass die Verbindung vom menschlichen Organismus synthetisiert werden kann. Cholin wurde daher vielfach als vitaminähnliche Substanz (Vitaminoid) klassifiziert.
Allerdings scheint eine gewisse Aufnahme von Cholin durch die Nahrung nötig zu sein. So konnte in einem Experiment gezeigt werden, dass eine Kunstnahrung mit extrem geringem Cholin-Gehalt zu Muskelschäden und Fettleber führt.
Für einige Tiere ist die Aufnahme von Cholin mit der Nahrung essentiell. Bei monogastrischen Tieren wird es auch durch die Nahrung aufgenommen, da Cholin als Bestandteil von Phosphatidylcholinen in der Zellmembran vorhanden ist. Wiederkäuer bilden hier eine Ausnahme, da Cholin nahezu vollständig im Pansen abgebaut wird.
Aufnahme und Vorkommen
| Lebensmittel | Cholin-Gehalt pro 100 g |
|---|---|
| Pflanzlich | |
| Erdnuss | 52 mg |
| Sojamilch | 23 mg |
| Linsen | 32 mg |
| Haferflocken | 32 mg |
| Vollkornweizen | 60 mg |
| Pilze | 16 mg |
| Blumenkohl | 40 mg |
| Brokkoli | 40 mg |
| Rosenkohl | 40 mg |
| Tierisch | |
| Milch | 14 mg |
| Käse | 15–25 mg |
| Fleisch | 65–108 mg |
| Ei (eines) | 150 mg |
| Fisch | 60–90 mg |
Die durchschnittliche Aufnahme von Cholin beträgt bei den meisten Menschen etwa 150 bis 600 mg pro Tag. Cholin kommt in zahlreichen Lebensmitteln vor. Tierische Lebensmittel wie Fleisch, Geflügel, Fisch, Milchprodukte und Eier enthalten höhere Mengen an Cholin. Bei pflanzlichen Lebensmitteln stellen Brokkoli, Kohlgemüse, Bohnen, Nüsse, Samen und Vollkorngetreide Cholin-Quellen dar.
Nahrungsmittel, die Betaine enthalten, können den Cholinbedarf senken. Zwar kann Betaine nicht zu Cholin umgewandelt werden, jedoch kann es als Methylgruppen-Spender wirken und verringert so den Cholinbedarf. Betain kann in großen Mengen in pflanzlicher Nahrung vorkommen (daher die Namensgebung, die sich von beets, also Rüben ableitet). Allerdings enthalten nur membranreiche Pflanzenteile wesentliche Mengen (bspw. Weizenkeime).
2019 erregte ein Meinungsbeitrag im British Medical Journal mediale Aufmerksamkeit. In diesem stellte die Autorin die These einer „Cholin-Krise“ in den Raum und dass der Trend hin zu einer veganen Ernährung zu vermehrtem Cholinmangel führen würde. Die Autorin ist Mitglied im „Meat Advisory Panel“, welches von der Fleischindustrie finanziell gefördert wird. Andere Ernährungswissenschaftler gehen davon aus, dass bei einer ausgewogenen und abwechslungsreichen veganen Ernährung der Cholinbedarf gedeckt werden kann.
In Lebensmitteln liegt Cholin sowohl in freier Form als auch gebunden als Sphingomyelin oder Phosphatidylcholin (Lecithin) vor. Es ist in Getreide (z.B. Weizenkeime), Sojabohnen, Gemüse und Nüssen enthalten. Die höchsten Gehalte sind in Eigelb, Rinder- und Schweineleber anzutreffen.
Bioverfügbarkeit
Darmbakterien formen zugeführtes Cholin zu Betain um. Dabei können die umgewandelten Mengen so erheblich sein, dass dieser Prozess Auswirkungen auf den Cholinbedarf hat.
Bedarf
| Altersgruppe | EFSA (2016) mg / Tag |
|---|---|
| Kleinkinder (7–11 Monate) | 300 |
| Kleinkinder (1–3 Jahre) | 140 |
| Kinder (4–6 Jahre) | 170 |
| Kinder (7–10 Jahre) | 250 |
| Jugendliche (11–14 Jahre) | 340 |
| Adoleszente (15–17 Jahre) | 400 |
| Erwachsene | 400 |
| Schwangere | 480 |
| Stillende | 520 |
Eine offizielle Zufuhrempfehlung auf Basis von exakten Daten und einem genauen ernährungswissenschaftlichen Verständnis von Cholin gibt es derzeit nicht.
Das amerikanische Food and Nutrition Board hat daher keine Angabe zum Estimated Average Requirement (EAR) aussprechen können, nur eine adäquate Zufuhr (AI). Für Erwachsene wurde die AI auf 550 mg/Tag für Männer und 425 mg/Tag für Frauen festgelegt. Diese Werte verhinderten in einer Studie negative Veränderungen der Leber. Allerdings verglich die Studie nur eine Cholin-freie Ernährung mit einer, die 550 mg pro Tag enthielt. Daraus wurde dann auch die AI für Kinder und Jugendliche interpoliert.
Bislang hat auch die EFSA nur einen Adequate Intake als Näherungswert festgelegt:
- 160 mg für Kleinkinder im Alter von 7 bis 11 Monaten
- 140 bis 340 mg für Kinder im Alter von 1 bis 14 Jahren
- 400 mg für Erwachsene sowie Jugendliche im Alter von 15 bis 17 Jahren
- 480 mg für Schwangere und 520 mg für stillende Frauen (aufgrund der erhöhten Cholinverluste über die Muttermilch)
Schwangere haben vermutlich einen erhöhten Cholinbedarf, aber auch für diesen gibt es nur Schätzwerte.
Das US-amerikanische Institute of Medicine der National Academy of Sciences gibt folgende Werte für Adequate Intake (AI) und Tolerable Upper Intake Level (UL) von Cholin an:
| Säuglinge und Kinder |
AI (mg/Tag) | UL (mg/Tag) | Männer | AI (mg/Tag) | UL (mg/Tag) | Frauen | AI (mg/Tag) | UL (mg/Tag) | Schwangere und Stillende |
AI (mg/Tag) | UL (mg/Tag) |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 0–6 Monate | 125 | – | 9–13 Jahre | 375 | 2000 | 9–13 Jahre | 375 | 2000 | Schwangere ≤ 18 Jahre |
450 | 3000 |
| 7–12 Monate | 150 | – | 14–18 Jahre | 550 | 3000 | 14–18 Jahre | 400 | 3000 | Schwangere 19–30 Jahre |
450 | 3500 |
| 1–3 Jahre | 200 | 1000 | 19–30 Jahre | 550 | 3500 | 19–30 Jahre | 425 | 3500 | Schwangere 31–50 Jahre |
450 | 3500 |
| 4–8 Jahre | 250 | 1000 | 31–50 Jahre | 550 | 3500 | 31–50 Jahre | 425 | 3500 | Stillende ≤ 18 Jahre |
550 | 3000 |
| 50–70 Jahre | 550 | 3500 | 50–70 Jahre | 425 | 3500 | Stillende 19–30 Jahre |
550 |
3500 | |||
| > 70 Jahre | 550 | 3500 | > 70 Jahre | 425 | 3500 | Stillende 31–50 Jahre |
550 |
3500 | |||
| |||||||||||
Die Rolle von Cholin als Methylgruppen-Spender scheint der Haupteinflussfaktor darauf zu sein, wie schnell eine Ernährung ohne Cholin zu pathologischen Mangelerscheinungen führt.
Metabolismus

Cholin kommt in den meisten Lebewesen vor. In Form seines Essigsäureesters bildet es den Neurotransmitter Acetylcholin, in Form seines Phosphorsäureesters ist es Bestandteil der Lecithine (Phosphatidylcholine) und außerdem Zwischenprodukt des Stoffwechsels.
Durch die Übertragung eines Acetyl-Restes auf das Cholin durch die
Cholin-Acetyltransferase
(EC
![]() 2.3.1.6) erfolgt die
Biosynthese des wichtigen
Neurotransmitters Acetylcholin. In Umkehrung dieser Reaktion ist die Acetylcholinesterase
für die Hydrolyse dieses Esters zu Essigsäure
und Cholin verantwortlich.
2.3.1.6) erfolgt die
Biosynthese des wichtigen
Neurotransmitters Acetylcholin. In Umkehrung dieser Reaktion ist die Acetylcholinesterase
für die Hydrolyse dieses Esters zu Essigsäure
und Cholin verantwortlich.
Cholin wird durch die Cholinkinase
(EC
![]() 2.7.1.32)
phosphoryliert. Das entstehende zwitterionige O-Phosphocholin dient
als Ausgangsstoff der Biosynthese von Phosphatidylcholinen, die essentieller Bestandteil von Biomembranen sind.
2.7.1.32)
phosphoryliert. Das entstehende zwitterionige O-Phosphocholin dient
als Ausgangsstoff der Biosynthese von Phosphatidylcholinen, die essentieller Bestandteil von Biomembranen sind.
Cholin kann weiterhin zu Betain, dem zwitterionigen Trimethylglycin, oxidiert werden, welches neben Folsäure, S-Adenosylmethionin und Vitamin B12 ein wichtiger Methylgruppenüberträger im Metabolismus ist.
Cholin wirkt außerdem als ein lipotroper Faktor und kann die Einlagerung von Fett in der Leber verhindern. Nach wissenschaftlicher Einschätzung der Europäischen Behörde für Lebensmittelsicherheit (EFSA) trägt Cholin zu einem normalen Lipidstoffwechsel und einer normalen Leberfunktion und einem normalen Stoffwechsel des Homocysteins bei. Dementsprechende gesundheitsbezogene Werbeaussagen sind bei Nahrungsmitteln mit genügend Cholinanteil in der gesamten Europäischen Union nach Verordnung (EG) Nr. 1924/2006 (Health Claims) zulässig. Dagegen gibt es keine Hinweise darauf, dass Cholin – wie auch Lecithin – bei Personen ohne Mangel zu einer Verbesserung des Gedächtnisses führt.
Verschiedene Ester des Cholins, z.B. das als Suxamethonium bekannte Succinyldicholin, wirken als Agonisten der Acetylcholin-Rezeptoren, ohne von vorhandenen Cholinesterasen schnell abgebaut werden zu können. Nach kurzer Erregung kommt es zu einer langanhaltenden Depolarisation und damit zur Muskelrelaxation.
Siehe auch
Literatur
- Wolfgang Herrmann, Rima Obeid (Hrsg.): Vitamins in the prevention of human diseases. Gruyter, 2011, ISBN 978-3-11-021448-2.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 21.12. 2025