
Natriumdisulfit
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK | Schweiz: 5 mg·m−3 (gemessen als einatembarer Staub)[4] | ||||||||
Natriumdisulfit, (Na2S2O5) auch Natriumpyrosulfit oder Natriummetabisulfit genannt, ist ein Natriumsalz der in freier Form nicht stabilen Dischwefligen Säure.
| Strukturformel | ||
|---|---|---|
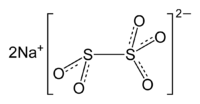
| ||
| Allgemeines | ||
| Name | Natriumdisulfit | |
| Andere Namen | ||
| Summenformel | Na2S2O5 | |
| Kurzbeschreibung | weißer bis gelblicher kristalliner Feststoff mit stechendem Geruch[2] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 231-673-0 | |
| ECHA-InfoCard | ||
| PubChem | ||
| DrugBank | ||
| Eigenschaften | ||
| Molare Masse | 190,11 g/mol | |
| Aggregatzustand | fest | |
| Dichte | 2,36 g/cm−3 bei 20 °C | |
| Schmelzpunkt | Zersetzung ab 150 °C | |
| Löslichkeit | leicht in Wasser (ca. 650 g/l bei 20 °C) | |
Natriumdisulfit kann namentlich leicht mit Natriumbisulfit verwechselt werden, einem älteren aber noch gebräuchlichen Namen für Natriumhydrogensulfit.
Synthese
Die Herstellung erfolgt durch thermische Dimerisierung (Kondensation) von Natriumhydrogensulfit unter Abspaltung von Wasser (1), oder durch Umsetzung von Schwefeldioxid und Natriumsulfit in Natronlauge (2):
Eigenschaften
Disulfite verfügen über eine recht lange, daher wenig stabile Schwefel-Schwefel-Bindung. In Wasser erfolgt daher leicht die Hydrolyse zu Natriumhydrogensulfit:
Beim Erhitzen des Salzes erfolgt eine thermische Zersetzung unter Abspaltung von Schwefeldioxid (SO2):
Verwendung

In Deutschland wird Natriumdisulfit als Lebensmittelzusatzstoff (E 223) vor allem als Konservierungsmittel und Antioxidationsmittel verwendet. Es wird in Trockenfrüchten, bei Meerrettichmasse, Frucht- und Gemüsezubereitungen, Meeresfrüchten, Kartoffelgerichten, Fertiggerichten, Fruchtsäften und Marmeladen eingesetzt. Auch in Kombination mit Sorbinsäure und Benzoesäure wird es verwendet. Es kann zur Diagnostik beim Sichelzelltest eingesetzt werden, um dem Hämoglobin bei der Sichelzellanämie den Sauerstoff zu entziehen und eine Sichelbildung zu beschleunigen.
Natriumdisulfit wird auch als Reduktionsmittel bei der Chemiefaserherstellung, zum Entgiften chromhaltiger Abwässer der Galvanobetriebe sowie in der Fotoindustrie und Bauchemie eingesetzt.[6]
Gesundheitshinweise / Risikobewertung
Bei den meisten Menschen wird Natriumdisulfit in den in Lebensmitteln vorhandenen Konzentrationen schnell durch ein körpereigenes Enzym abgebaut, würde aber sonst zu Übelkeit, Erbrechen, Durchfall und Kopfschmerzen führen.[5] Bei Asthmatikern kann es Sulfitasthma auslösen; außerdem sind allergische und allergieähnliche Reaktionen möglich, wenn auch selten.[5] In Lebensmitteln zerstört Natriumdisulfit Vitamin B1 (Thiamin).[6]
Natriumdisulfit wurde 2014 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Dabei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Natriumdisulfit waren die Besorgnisse bezüglich Umweltexposition, Exposition empfindlicher Bevölkerungsgruppen, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Stoffe. Die Neubewertung fand ab 2014 statt und wurde von Ungarn durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[7][8]
Einzelnachweise
- ↑ Eintrag zu
 SODIUM METABISULFITE in der
CosIng-Datenbank der EU-Kommission.
SODIUM METABISULFITE in der
CosIng-Datenbank der EU-Kommission.
- ↑ Hochspringen nach: a
b c Eintrag zu
 Natriumdisulfit in der GESTIS-Stoffdatenbank
des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. (JavaScript erforderlich)
Natriumdisulfit in der GESTIS-Stoffdatenbank
des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. (JavaScript erforderlich)
- ↑ Eintrag zu
 Disodium disulphite im
Classification and Labelling Inventory der
Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die
harmonisierte Einstufung und Kennzeichnung
Disodium disulphite im
Classification and Labelling Inventory der
Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die
harmonisierte Einstufung und Kennzeichnung  erweitern.
erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva):
 Grenzwerte – Aktuelle MAK- und
BAT-Werte (Suche nach 7681-57-4 bzw. Natriumdisulfit).
Grenzwerte – Aktuelle MAK- und
BAT-Werte (Suche nach 7681-57-4 bzw. Natriumdisulfit).
- ↑ Hochspringen nach: a
b zusatzstoffe-online.de:
 Natriumdisulfit.
Natriumdisulfit.
- ↑ das-ist-drin.de:
 Natriummetabisulfit; Natriumdisulfit.
Natriummetabisulfit; Natriumdisulfit.
- ↑ Europäische Chemikalienagentur
(ECHA):
 Substance Evaluation Report und
Substance Evaluation Report und
 Conclusion Document.
Conclusion Document.
- ↑ Community rolling action plan (CoRAP) der
Europäischen Chemikalienagentur (ECHA):
 Disodium disulphite.
Disodium disulphite.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 18.11. 2025

