
Chlormethan
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK |
| ||||||||
| Treibhauspotential | 15 (bezogen auf 100 Jahre) | ||||||||
Methylchlorid oder Chlormethan ist ein farbloses, schwach süßlich riechendes, gesundheitsschädliches und leicht brennbares Gas.
| Strukturformel | |
|---|---|
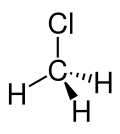 | |
| Keilstrichformel zur Verdeutlichung der Geometrie | |
| Allgemeines | |
| Name | Chlormethan |
| Andere Namen |
|
| Summenformel | CH3Cl |
| Kurzbeschreibung | farbloses, etherisch riechendes Gas |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 74-87-3 |
| EG-Nummer | 200-817-4 |
| ECHA-InfoCard | 100.000.744 |
| PubChem | 6327 |
| ChemSpider | 6087 |
| Eigenschaften | |
| Molare Masse | 50,49 g/mol |
| Aggregatzustand | gasförmig |
| Dichte |
|
| Schmelzpunkt | −97,4 °C |
| Siedepunkt | −23,8 °C |
| Dampfdruck |
|
| Löslichkeit | schlecht in Wasser (5 g/l bei 20 °C) |
| Dipolmoment | 1,892 D (6,31 · 10−30 C·m) |
| Thermodynamische Eigenschaften | |
| ΔHf0 | −81,9 kJ/mol (gasförmig) |
Vorkommen
Methylchlorid ist die häufigste chlorhaltige Verbindung in der Atmosphäre. Neben den industriellen Quellen tragen natürliche Emissionen aus immergrünen Bäumen, aber auch aus anderen Pflanzen wie Kartoffeln, zu erheblichen Mengen bei.
Gewinnung
Chlormethan kann durch Erhitzen von Chlor und Methan auf 400–500 °C erzeugt werden. Bei dieser Temperatur findet eine schrittweise radikalische Substitution bis hin zu Tetrachlormethan statt. Alle Reaktionsschritte verlaufen exotherm.
mit ΔRH = −103,5 kJ·mol−1
mit ΔRH = −102,5 kJ·mol−1
mit ΔRH = −99,2 kJ·mol−1
mit ΔRH = −94,8 kJ·mol−1
- Methan reagiert mit Chlor unter Bildung von Chlorwasserstoff zunächst zu Chlormethan, und weiter zu Dichlormethan, Trichlormethan (Chloroform) und schließlich Tetrachlormethan.
Das Ergebnis des Prozesses ist eine Mischung der vier Chlormethane, welche durch Destillation getrennt werden können.
Ein zweites technisches Verfahren ist die Methanolhydrochlorierung, d.h. Methanol wird mit Chlorwasserstoff zu Chlormethan umgesetzt. Die Reaktion findet katalysiert in der Gas- oder Flüssigphase statt. Die Umsetzung verläuft schwach exotherm.
mit ΔRH = −33 kJ·mol−1
Eigenschaften
Physikalische Eigenschaften
Chlormethan ist ein farbloses Gas. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in kPa, T in K) mit A = 6,9, B = 1449 und C = 48 im Temperaturbereich von 308 bis 373 K. Die kritische Temperatur beträgt 143 °C, der kritische Druck 66,7 bar und die kritische Dichte 0,353 g·cm−3. Die Mischbarkeit mit Wasser ist begrenzt. Mit steigender Temperatur sinkt die Löslichkeit von Chlormethan in Wasser.
| Löslichkeit von Chlormethan in Wasser | ||||||||||||
| Temperatur | °C | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| Chlormethan in Wasser | in Ma-% | 3,42 | 3,19 | 3,01 | 2,88 | 2,79 | 2,72 | 2,68 | 2,66 | 2,67 | 2,69 | 2,73 |
Chemische Eigenschaften
Chlormethan bildet mit Wasser ein schneeartiges festes Gashydrat mit der Zusammensetzung CH3Cl·6H2O, welches schon bei 7,5 °C und Normaldruck zu seinen Komponenten zerfällt. Bei Raumtemperatur erfolgt in Wasser eine langsame Hydrolyse, die in Gegenwart von Basen wesentlich beschleunigt wird. Mineralsäuren ergeben keinen Einfluss auf die Hydrolysegeschwindigkeit. Mit Alkali- oder Erdalkalimetallen wie auch Zink und Aluminium werden entsprechende metallorganische Verbindungen gebildet.
Die Umsetzung mit einem Natrium-Blei-Amalgam führt zur Bildung von Tetramethylblei.
Die als Müller-Rochow-Synthese bekannte Reaktion mit Silizium ergibt die Methylchlorsilane. Als Methylierungsreagenz werden mit Ammoniak und Aminen die entsprechenden Methylamine gebildet. Analog führt die Reaktion mit Hydroxygruppen enthaltenden Verbindungen zu den entsprechenden Methylethern, wie z.B. die Herstellung von Methylcellulose aus Cellulose.
Sicherheitstechnische Kenngrößen
Die Verbindung bildet leicht entzündliche Gas-Luft-Gemische. Der Explosionsbereich liegt zwischen 7,6 Vol.‑% (160 g/m3) als untere Explosionsgrenze (UEG) und 19 Vol.‑% (410 g/m3) als obere Explosionsgrenze (OEG). Die Grenzspaltweite wurde mit 1 mm (50 °C) bestimmt. Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA. Die Zündtemperatur beträgt 625 °C. Der Stoff fällt somit in die Temperaturklasse T1.
Verwendung
Chlormethan wird als Methylierungsmittel in der organischen Chemie, als Polymerisationsmedium für Butylkautschuk (verflüssigt bei ca. −90 °C), zur Veretherung von Alkoholen und Phenolen sowie bei der Silikonherstellung eingesetzt. Seine hohe Verdampfungsenthalpie ermöglicht auch einen Einsatz als Kältemittel. Früher wurde es zur Narkose, aber auch als lokales Kälteanästhetikum verwendet.
Toxizität und Risikobewertung
Das betäubende Gas löst Störungen des Zentralnervensystems aus und schädigt Leber, Niere und Herz. Methylchlorid gilt als Stoff mit begründetem Verdacht auf krebserzeugendes Potential und der Fruchtschädigung.
Chlormethan wurde 2012 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Chlormethan waren die Besorgnisse bezüglich der Einstufung als CMR-Substanz, hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) sowie als potentieller endokriner Disruptor. Die Neubewertung fand ab 2012 statt und wurde von Italien durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 05.11. 2024


