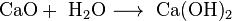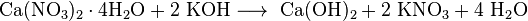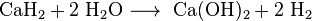Calciumhydroxid
| Sicherheitshinweise | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Toxikologische Daten | 7340 mg·kg−1 (LD50, Ratte, oral) | |||||||||||||||
Calciumhydroxid (auch: gelöschter Kalk, Löschkalk, (Weiß)Kalkhydrat, Hydratkalk) ist das Hydroxid des Calciums.
Vorkommen
Calciumhydroxid kommt in der Natur auch als Mineral Portlandit vor.
Gewinnung und Darstellung
Calciumhydroxid entsteht unter starker Wärmeentwicklung (exotherme Reaktion) beim Versetzen von Calciumoxid mit Wasser. Diesen Vorgang nennt man auch Kalklöschen. Die Wärmeentwicklung ist so stark, dass das Wasser zum Teil auch verdampft (umgangssprachlich als „Rauchen“ bezeichnet).
Einen Überblick über die Umwandlungsprozesse zwischen verschiedenen Calciumverbindungen (technischer Kalkkreislauf) gibt folgendes Schaubild:
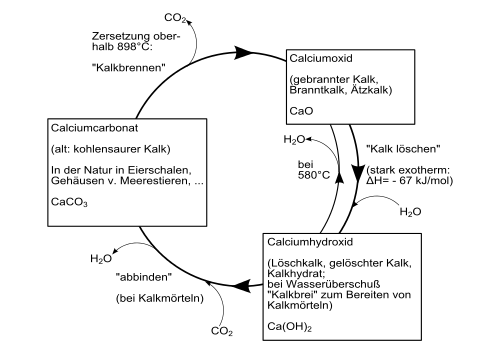
Weiterhin ist die Darstellung durch Reaktion von wässrigen Calciumsalzlösungen mit Alkalilaugen möglich (zum Beispiel Calciumnitrat mit Kaliumhydroxid).
Calciumhydrid oder Calcium selbst reagiert mit Wasser heftig unter Bildung von Calciumhydroxid und Wasserstoff.
Eigenschaften

Calciumhydroxid ist ein farbloses Pulver, welches sich nur wenig in Wasser löst, wobei die Lösung stark basisch reagiert. Die Löslichkeit ist temperaturabhängig und sinkt bei steigender Temperatur: 1860 mg/l bei 0 °C; 1650 mg/l bei 20 °C und 770 mg/l bei 100 °C. Bei 580 °C zersetzt es sich, wobei Calciumoxid und Wasser entstehen. Calciumhydroxid besteht aus hexagonalen Kristallen mit einer Kristallstruktur vom Cadmiumiodid-Typ (a = 3,584, c = 4,896 A).
Calciumhydroxid ist basisch. Der pH-Wert einer gesättigten Lösung liegt bei 11-12,6.
| Kristallstruktur | |
|---|---|
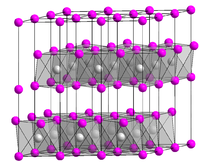 | |
| __ Ca2+ __ OH− | |
| Allgemeines | |
| Name | Calciumhydroxid |
| Andere Namen |
|
| Verhältnisformel | Ca(OH)2 |
| CAS-Nummer | 1305-62-0 |
| Kurzbeschreibung | farbloser, geruchloser Feststoff |
| Eigenschaften | |
| Molare Masse | 74,10 g/mol |
| Aggregatzustand | fest |
| Dichte | 2,24 g/cm3 (20 °C) |
| Schmelzpunkt | Zersetzung bei 550 °C |
| Löslichkeit | schlecht in Wasser (1,7 g/l bei 20 °C) |
Verwendung
Der Haupteinsatzzweck von Calciumhydroxid ist die Zubereitung von Mörtel im Bauwesen. Es findet dort unter dem Namen Weißkalkhydrat Verwendung (DIN 1060). Kalkputze bestehen aus Mischungen von Calciumhydroxid und Sand. Letzterer kann auch in Form von gemahlenem Kalkstein beigefügt werden.
Calciumhydroxid dient auch als Zwischenprodukt zur Herstellung von Chlorkalk und Natronlauge aus Soda.
Weiterhin wird es als Medikament in der Zahnmedizin verwendet, vor allem zur Desinfektion von Wurzelkanälen und Kavitäten und zur Anregung der Dentin-Neubildung.
Es ist auch Bestandteil des Atemkalks, welche in Narkosegeräten oder Tauchgeräten mit Rückatmung zum Herausfiltern von Kohlenstoffdioxid aus der Ausatemluft verwendet wird.
Eine weitere Verwendung findet Calciumhydroxid als Pflanzenschutzmittel im Obstbau. Hier wird es zum Beispiel als Fungizid (ein Mittel gegen Pilzbefall, etwa Obstbaumkrebs) eingesetzt.
Die ätzende Wirkung, welche auch diverse Krankheitserreger zerstört, ist der Grund, warum früher gelöschter Kalk zum Desinfizieren von Ställen (das „Kalken“ der Ställe) benutzt wurde.
In der Lebensmittelindustrie wird es als Säureregulator Lebensmitteln zugesetzt und ist in der Europäische Union als Lebensmittelzusatzstoff der Bezeichnung E 526 ohne Höchstmengenbeschränkung (quantum satis) für Lebensmittel allgemein zugelassen.
Der gelöschte Kalk wird unter anderem als Alternative zum Kalkstein in der Rauchgasentschwefelung eingesetzt, da es mit Schwefelsäure Calciumsulfat (Gips) bildet. Die Einsatzmenge ist hierbei ca. 1,8-fach geringer als für Kalkstein. Der dabei gewonnene Gips hat einen Weißgrad von 80 % und kann kommerziell weiterverwendet werden. Durch seine hohe Reaktivität werden geringere Verbrauchmengen benötigt. Nachteil ist sein deutlich höherer Preis gegenüber Kalkstein.
Kalk wird auch zur Verbesserung der Tragfähigkeit von Baugrund eingesetzt. Ein Boden mit zu hohem Wassergehalt und daraus resultierender geringer Tragfähigkeit, schlechter Verdichtbarkeit kann durch das Untermischen von 2–4 % MA Kalk verbessert werden. Der Kalk bindet einen Teil des Wassers und verbessert so unter anderem die Plastizität, die Verdichtbarkeit und die Tragfähigkeit. Deshalb ist die Bodenverbesserung mit Kalk ein Verfahren zur sofort erreichbaren Verbesserung der Einbaufähigkeit und Erleichterung der Ausführung von Bauarbeiten.
Kalkwasser ist die (nahezu) gesättigte Lösung von Calciumhydroxid und dient als klare Flüssigkeit dem Nachweis von Kohlenstoffdioxid.
Suspensionen in Wasser sind:
- Fettkalk (Sumpfkalk): eine cremig-steife Masse – Baustoff: Kalkmörtel
- Kalkmilch: eine weißliche, milchartige Flüssigkeit, die sich aber entmischt – Kalkfarbe, Neutralisation von Säuren, Entcarbonisierung, Rauchgasentschwefelung
Sicherheitshinweise
Gebrannter (ungelöschter) Kalk (Calciumoxid, Branntkalk) und gelöschter Kalk sind reizend, Kontakt mit den Augen kann zu ernsten Augenschäden führen. Ungelöschter Kalk kann unter Wasserzufuhr Brände verursachen.
Historisches
Die exotherme Reaktion des Löschkalks galt von der Antike bis in die Frühe Neuzeit als eines der grössten alltäglichen Rätsel und fand die unterschiedlichsten Erklärungen: Während der Kirchenvater Augustinus von Hippo (354 – 430) in seinem „Gottesstaat“ (21, 4) das Phänomen als eine Art Gottesbeweis ansieht, bemühten sich die Naturphilosophen das Phänomen nach ihren jeweiligen Vorstellungen zu deuten. Als prominente Beispiele sind zu nennen:
Seneca der Jüngere und die Stoa
Entsprechend der stoischen Kosmologie deutete der römische Philosoph Seneca der Jüngere († 65 n. Chr) das Kalklöschen entsprechend der Vier-Elemente-Lehre des Aristoteles. Das Calciumoxyd ist für ihn nach dem Brennen eine Art „feuriger Stein“, welcher die Hitze an das ihn durchdringende Wasser abgibt.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 29.12. 2022