Nickeltetracarbonyl
| Sicherheitshinweise | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| MAK |
Schweiz: 0,05 ml/m3 bzw. 0,35 mg/m3 [3] | |||||||||
Nickeltetracarbonyl ist eine farblose Flüssigkeit. Diese chemische Verbindung gehört zu der Gruppe der Metallcarbonyle. Von besonderer Bedeutung ist Nickeltetracarbonyl bei der Herstellung von Reinstnickel und als Katalysator.
| Strukturformel | ||
|---|---|---|
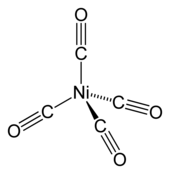
| ||
| Allgemeines | ||
| Name | Nickeltetracarbonyl | |
| Andere Namen |
| |
| Summenformel | [Ni(CO)4] | |
| Kurzbeschreibung | farblose Flüssigkeit[1] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | | |
| EG-Nummer | 236-669-2 | |
| ECHA-InfoCard | | |
| PubChem | | |
| Eigenschaften | ||
| Molare Masse | 170,73 g/mol | |
| Aggregatzustand | flüssig | |
| Dichte | 1,32 g/cm3[1] | |
| Schmelzpunkt | −25 °C[1] | |
| Siedepunkt | 43 °C[1] | |
| Dampfdruck | 425 hPa (20 °C)[1] | |
| Löslichkeit | sehr schlecht in Wasser (2 mg/l bei 20 °C)[1] | |
Geschichte
Nickeltetracarbonyl wurde 1890 vom deutsch-englischen Chemiker Ludwig Mond entdeckt.
Gewinnung und Darstellung
Nickeltetracarbonyl bildet sich beim Kontakt von fein verteiltem Nickelpulver mit Kohlenmonoxid ab 60 °C.[4] Nach seinem Entdecker nennt man diese Synthese auch Mond-Verfahren, das so gewonnene Nickel auch „Mond-Nickel“:
Die Reaktion ist reversibel. Ab 180 °C zerfällt die Verbindung in die Ausgangssubstanzen.[4]
Chemische Eigenschaften
Nickeltetracarbonyl entzündet sich bei über 60 °C an der Luft. Es reagiert heftig mit Oxidationsmitteln (Explosionsgefahr). Es zersetzt sich oberhalb von ca. 160 °C in elementares Nickel und Kohlenmonoxid. In Nickeltetracarbonyl hat Nickel die in Verbindungen sonst seltene Oxidationszahl 0.
Verwendung
Reinstnickel mit einem Gehalt > 99,9 % wird durch thermische Zersetzung von (destillativ leicht zu reinigendem) Nickeltetracarbonyl dargestellt (siehe Mond-Verfahren). Nickeltetracarbonyl dient vielfach als Grundstoff für metallorganische Ni-Verbindungen, die u. a. als vielseitige Katalysatoren benutzt werden. Die Verbindung dient auch als Katalysator bei der Hydrocarboxylierung.
Sicherheitshinweise
Nickeltetracarbonyl ist akut toxisch und nimmt daher unter den Nickelverbindungen eine Sonderstellung ein. Es wird nicht unter der Begrifflichkeit „Nickel und seine Verbindungen“ subsumiert und verfügte lange Zeit über einen eigenen Grenzwert. In Tierversuchen erwies sich Nickeltetracarbonyl als krebserzeugend (K 2).[5] An der Luft kann es sich selbst entzünden (Explosionsgefahr).
Nickeltetracarbonyl hat starke irritative Wirkungen beim Menschen, in Einzelfällen kann eine BK-Nr. 4302 in Betracht kommen. Die erste Liste mit MAK-Werten von 1958 enthielt einen MAK-Wert für Nickeltetracarbonyl in Höhe von 0,7 mg/m3. Dieser wurde 1980 ausgesetzt. Ab 1983 galt bis zu ihrer Aufhebung 1995 eine Technische Richtkonzentration (TRK) in gleicher Höhe. Die Aufhebung erfolgte nach einer Überprüfung der TRK mit dem Ergebnis, dass der Stoff nur noch eine geringe technische Bedeutung hatte.[5]
Trivia
Nickeltetracarbonyl ist aufgrund seiner hohen Toxizität auch unter dem Namen liquid death bekannt.[6]
Weblinks
- International Chemical Safety Card (ICSC) für
 Nickel carbonyl bei der
International Labour Organization (ILO)
Nickel carbonyl bei der
International Labour Organization (ILO)
Einzelnachweise
- ↑ Hochspringen nach: a b
c d e
f g Eintrag zu
 Nickeltetracarbonyl in der
GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen
Unfallversicherung. (JavaScript erforderlich)
Nickeltetracarbonyl in der
GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen
Unfallversicherung. (JavaScript erforderlich)
- ↑ Eintrag zu
 Tetracarbonylnickel im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
Tetracarbonylnickel im
Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA).
Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung
 erweitern.
erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva):
 Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 13463-39-3 bzw. Nickeltetracarbonyl)
Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 13463-39-3 bzw. Nickeltetracarbonyl)
- ↑ Hochspringen nach: a b D.E.G. Kerfoot: Nickel,
in: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2012;
doi:
 10.1002/14356007.a17_157.
10.1002/14356007.a17_157.
- ↑ Hochspringen nach: a b Deutsche Gesetzliche
Unfallversicherung e.V. (DGUV):
 BK Report – Nickel und seine
Verbindungen.
BK Report – Nickel und seine
Verbindungen.
- ↑
 Urban Dictionary: liquid death. (amerikanisches Englisch).
Urban Dictionary: liquid death. (amerikanisches Englisch).


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 23.03. 2025



