
Anisol
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| Toxikologische Daten | 3,7 g/kg (LD50, Ratte, oral) | |||||||
Anisol ist eine charakteristisch riechende, farblose, entzündliche Flüssigkeit. Da Anisol formal als Ether aus Phenol und Methanol aufgefasst werden kann, bezeichnet man es auch als Methylphenylether oder Methoxybenzol.
| Strukturformel | ||
|---|---|---|
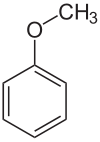
| ||
| Allgemeines | ||
| Name | Anisol | |
| Andere Namen |
| |
| Summenformel | C7H8O | |
| Kurzbeschreibung | farblose Flüssigkeit mit angenehmem Geruch | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 202-876-1 | |
| ECHA-InfoCard | ||
| PubChem | ||
| ChemSpider | ||
| Eigenschaften | ||
| Molare Masse | 108,14 g/mol−1 | |
| Aggregatzustand | flüssig | |
| Dichte | 0,99 g/cm3 (20 °C) | |
| Schmelzpunkt | −37 °C | |
| Siedepunkt | 154 °C | |
| Dampfdruck |
| |
| Löslichkeit |
| |
| Dipolmoment | 1,38(7) D (4,6 · 10−30 C · m) | |
| Brechungsindex | 1,516 (20 °C) | |
Darstellung und Gewinnung
Die Produktion von Anisol erfolgt durch die Veretherung von Phenol bzw. Phenolaten mit Dimethylsulfat oder Methylchlorid (Ethersynthese nach Williamson):
Vorkommen
.jpg)
Anisol ist ein eukaryotischer Metabolit, der bei einer Stoffwechselreaktion im Reich der Blütenpflanzen, Koniferen und anderen Gymnospermen, gebildet wird. Viele dieser Pflanzen sind für ihre Duftstoffe bekannt z.B.: Orchideen (Aerangis appendiculata, Aeranthes grandiflora, Bollea coelestis, Brassavola digbyana, Brassia verucosa, Cattleya lawrenceana, Dendrobium chrysotoxum, Dracula chestertonii, Encyclia fragrans, Epidendrum lacertinum, Liparis viridiflora, Masdevallia glandulosa, Nigritella nigra), Französischer Estragon (Artemisia dracumculus var.), Wildtulpe (Tulipa turkestanica), Neotropische Palmengattung (Asterogyne martiana), Weißer Ingwer („white ginger lily“), Kobushi-Magnoli, Rote Mangrove (Rhizophora mangle), Riesenbovist (Calvatia gigantea), Himbeere (Rubus idaeus), China-Rose (Rosa chinensis), Eidechsenwurz (Sauromatum guttatum), Kopfiger Thymian (Thymus capitatus).
Eigenschaften
Physikalische Eigenschaften
Anisol ist eine angenehm riechende, farblose Flüssigkeit, die bei Normaldruck bei 154 °C siedet. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,17726, B = 1489,756 und C = −69,607 im Temperaturbereich von 383,03 bis 437,26 K. Der Schmelzpunkt der Verbindung liegt bei −37 °C.
| Eigenschaft | Typ | Wert [Einheit] | Bemerkungen |
|---|---|---|---|
| Standardbildungsenthalpie | ΔfH0liquid ΔfH0gas |
−120,0 kJ·mol−1 −76,69 kJ·mol−1 |
als Flüssigkeit als Gas |
| Verbrennungsenthalpie | ΔcH0liquid | −3778 kJ·mol−1 | |
| Wärmekapazität | cp | 199,0 J·mol−1·K−1 (25 °C) 1,84 J·g−1·K−1 (25 °C) 176,98 J·mol−1·K−1 (160 °C) 1,64 J·g−1·K−1 (160 °C) |
als Flüssigkeit als Gas |
| Kritische Temperatur | Tc | 646,1 K[17] | |
| Kritischer Druck | pc | 42,22 bar | |
| Kritische Dichte | ρc | 2,93 mol·l−1 | |
| Schmelzenthalpie | ΔfH | 12,89 kJ·mol−1 | beim Schmelzpunkt |
| Verdampfungsenthalpie | ΔVH | 38,97 kJ·mol−1 | beim Normaldrucksiedepunkt |
Die Temperaturabhängigkeit der Verdampfungsenthalpie lässt sich entsprechend der Gleichung ΔVH0=A·e(−βTr)(1−Tr)β (ΔVH0 in kJ/mol, Tr =(T/Tc) reduzierte Temperatur) mit A = 63,45 kJ/mol, β = 0,2787 und Tc = 644,1 K im Temperaturbereich zwischen 298 K und 427 K beschreiben.
Chemische Eigenschaften
In Gegenwart von Luftsauerstoff, insbesondere bei der Lagerung neigt die Verbindung zur Bildung von Peroxiden. In Gegenwart von starken Säuren, wie Iodwasserstoffsäure erfolgt eine Etherspaltung.
Sicherheitstechnische Kenngrößen
Anisol bildet entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 41 °C. Der Explosionsbereich liegt zwischen 1,2 Vol.‑% (54 g/m³) als untere Explosionsgrenze (UEG) und 6,3 Vol.‑% (283 g/m³) als obere Explosionsgrenze (OEG). Die Grenzspaltweite wurde mit 0,82 mm bestimmt. Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB. Die Zündtemperatur beträgt 475 °C. Der Stoff fällt somit in die Temperaturklasse T1.
Verwendung
Verwendet wird Anisol als Lösungsmittel, Wärmeübertragungsmittel (zwischen 150 und 260 °C) und Ausgangsstoff für die Synthese organischer Verbindungen wie beispielsweise Arzneimitteln und Riechstoffen.
Anisol ist mit begrenzter Konzentration als Zusatz zu Lebensmitteln und Kosmetika zugelassen.
Verwandte Strukturen
Namentlich wie auch strukturell leiten sich vom Anisol durch Einführung eines Kohlenstoffatoms drei weitere Verbindungen ab: Anisalkohol, Anisaldehyd, Anissäure. Die Darstellung von Anisaldehyd erfolgt mittels Vilsmeier-Formylierung.
–CH2OH –CHO –COOH 
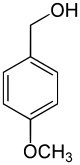
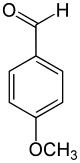
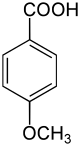
Anisol Anisalkohol Anisaldehyd Anissäure
Zu den Derivaten zählen auch:
- Anisolsulfonsäuren
- Phenetol (Ethoxybenzol)
- Anisidine (Aminoanisole)
- Methylanisole
- Nitroanisole
- Thioanisol (Phenolthioether)


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 08.03. 2025

