
Schwefeldichlorid
| Sicherheitshinweise | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
Schwefeldichlorid ist eine chemische Verbindung aus der Gruppe der Schwefelchloride. Es ist eine dunkelrote, toxische, hydrolyseempfindliche Flüssigkeit mit charakteristischem, an Chlor erinnerndem Geruch.
| Strukturformel | ||
|---|---|---|
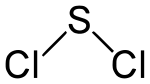 | ||
| Allgemeines | ||
| Name | Schwefeldichlorid | |
| Andere Namen |
| |
| Summenformel | SCl2 | |
| Kurzbeschreibung | rot-braune Flüssigkeit mit stechendem Geruch | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | 10545-99-0 | |
| EG-Nummer | 234-129-0 | |
| ECHA-InfoCard | 100.031.014 | |
| PubChem | 25353 | |
| Eigenschaften | ||
| Molare Masse | 102,97 g/mol | |
| Aggregatzustand | flüssig | |
| Dichte | 1,62 g/cm3 (bei 15 °C) | |
| Schmelzpunkt | −125 °C | |
| Siedepunkt | 59,5 °C | |
| Dampfdruck | 218 hPa (20 °C) | |
| Löslichkeit | reagiert mit Wasser | |
| Brechungsindex | 1,557 (14 °C) | |
Geschichte
Eine der ersten Anwendungen von Schwefeldichlorid erfolgte 1846. Damals nutzte Alexander Parkes in Schwefelkohlenstoff (CS2) gelöstes Schwefeldichlorid zur Kaltvulkanisation von Kautschuk. Während des Ersten Weltkrieges wurde Schwefeldichlorid zur Herstellung des Kampfstoffes S-Lost verwendet.
Gewinnung und Darstellung
Im Labor wird Schwefeldichlorid durch Umsetzung von Dischwefeldichlorid mit Chlorgas in Gegenwart von etwas FeCl2 oder FeCl3 als Katalysator hergestellt. Ebenfalls möglich ist die direkte Umsetzung von Schwefel mit Chlor, wobei ein Gemisch aus Dischwefeldichlorid und Schwefeldichlorid erhalten wird. Eine Trennung der beiden Flüssigkeiten kann durch Destillation unter Schutzgasatmosphäre erfolgen.
Eigenschaften
Schwefeldichlorid ist mit einer Bildungsenthalpie von −49 kJ/mol eine mäßig exotherme Verbindung. Sie ist bei Raumtemperatur nicht stabil und zersetzt sich teilweise in einer Gleichgewichtsreaktion zu Dischwefeldichlorid und Chlor. Eine Stabilisierung ist durch Zugabe von etwas Phosphortrichlorid oder Phosphorpentachlorid möglich.
Schwefeldichlorid schmilzt inkongruent bei −125 °C (nach anderer Quelle kongruent bei −70 °C). Es verhält sich dimorph, indem es aus der unterkühlten Schmelze zur Bildung einer weiteren, metastabilen Modifikation kommen kann, die sich bei Aufheizung im Bereich von −150 bis −135 °C exotherm in die strukturanalysierte Form umwandelt. Der eutektische Punkt, liegt bei ca. 60 Atom-% Cl und −144 °C.
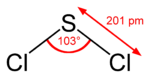
Schwefeldichlorid besitzt C2v-Symmetrie. Der Bindungswinkel zwischen Cl-S-Cl beträgt etwa 103 Grad, die Bindungslänge d(Cl–S) = 2,01 Å.
Verwendung
Schwefeldichlorid raucht an feuchter Luft unter Bildung von HCl. Es kann als Sulfidierungs- und Chlorierungsmittel in der Synthese verwendet werden. Mit ungesättigten Verbindungen wie Allylphenylethern oder Allylphenolen reagiert SCl2 zu den entsprechenden Thiaheterocyclen bzw. Sulfonen.
Sicherheitshinweise
Da mit Schwefeldichlorid auf relativ einfache Weise die Herstellung von Senfgas möglich ist, werden Produktion, Verwendung und vor allem Ausfuhr gesetzlich geregelt und überwacht.
Nachweis
SCl2 ist von C2v-Symmetrie (zweizählige Achse und zwei Spiegelebenen). In dieser Punktgruppe sind alle 3 Fundamentalschwingungen (symmetrische und asymmetrische Valenzschwingung sowie die Deformationsschwingung) IR-aktiv und Raman-erlaubt. Das Ramanspektrum kann zur Prüfung der Reinheit verwendet werden.
Literatur
- Ralf Steudel, David Scheschkewitz: Chemistry of the Non-Metals: Syntheses – Structures – Bonding – Applications. 2. Auflage, de Gruyter, Berlin / Boston 2020, ISBN 978-3-11-057805-8.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 21.04. 2026


