
Phosphorpentachlorid
| Sicherheitshinweise | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| MAK | DFG/Schweiz: 1 mg/m3 (gemessen als einatembarer Staub) | |||||||||
| Toxikologische Daten | 660 mg/kg (LD50, Ratte, oral) | |||||||||
Phosphorpentachlorid ist eine farblose, hygroskopische kristalline Masse von ätzendem Geruch. Es ist durch teilweisen Zerfall in Phosphortrichlorid und Chlor meist gelblich oder grünlich gefärbt.
| Strukturformel | ||
|---|---|---|
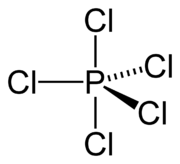
| ||
| Allgemeines | ||
| Name | Phosphorpentachlorid | |
| Andere Namen | Phosphor(V)-chlorid | |
| Summenformel | PCl5 | |
| Kurzbeschreibung | farbloser bis gelblicher Feststoff mit stechendem Geruch | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | ||
| EG-Nummer | 233-060-3 | |
| ECHA-InfoCard |
| |
| PubChem | ||
| Eigenschaften | ||
| Molare Masse | 208,24 g/mol | |
| Aggregatzustand | fest | |
| Dichte | 2,1 g/cm3 | |
| Schmelzpunkt |
| |
| Sublimationspunkt | 162,2 °C | |
| Dampfdruck | 20 Pa (20 °C) | |
| Löslichkeit | heftige Zersetzung in Wasser | |
Gewinnung und Darstellung
Die technische Darstellung von Phosphorpentachlorid erfolgt durch Chlorierung von Phosphortrichlorid in einer Gleichgewichtsreaktion:
Dabei werden die Edukte in mit Blei ausgekleideten Türmen im Gegenstromverfahren zur Reaktion gebracht.
Eigenschaften und Verwendung
Mit Wasser zersetzt sich der Stoff zu Phosphorsäure und Chlorwasserstoff:
Schon bei Normaltemperatur dissoziiert das Pentachlorid zum Phosphortrichlorid unter Abgabe von Chlor. Bei Normaldruck schmilzt Phosphorpentachlorid nicht, sondern sublimiert ab etwa 100 °C. In einer geschlossenen Apparatur schmilzt es unter Überdruck bei 148–160,5 °C. Kristallines festes Phosphorpentachlorid ist ionisch aufgebaut: [PCl4]+[PCl6]−.
Generell dient Phosphorpentachlorid als Chlorierungsmittel, da es sehr leicht Chlor abgibt. Es werden z.B. Carbonsäuren zum entsprechenden Säurechlorid umgesetzt. Durch Reaktion mit Benzophenon kann Dichlordiphenylmethan dargestellt werden.
Sicherheitshinweise
Phosphorpentachlorid ist sehr giftig und reagiert heftig mit Wasser, Metalloxiden, Metallpulvern und organischen Stoffen unter Hitzeentwicklung und Abspaltung giftiger Gase wie Phosphorylchlorid, Chlorwasserstoff und Chlorgas. Des Weiteren reagiert Phosphorpentachlorid mit vielen Säuren und deren Salzen zu den entsprechenden Säurechloriden. So bildet sich aus Carbonaten und Phosphorpentachlorid das äußerst giftige Phosgen.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 02.05. 2026


