
Kaliumchlorid
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| Toxikologische Daten | 2600 mg/kg (LD50, Ratte, oral) | ||||||||
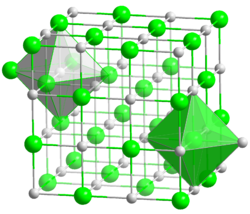
| Kristallstruktur | ||
|---|---|---|
| ||
| __ K+ __ Cl− | ||
| Kristallsystem | kubisch | |
| Raumgruppe | Fm3m (Nr. 225) | |
| Koordinationszahlen | K[6], Cl[6] | |
| Allgemeines | ||
| Name | Kaliumchlorid | |
| Andere Namen |
| |
| Verhältnisformel | KCl | |
| Kurzbeschreibung | farb- und geruchloser Feststoff | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | 7447-40-7 | |
| EG-Nummer | 231-211-8 | |
| ECHA-InfoCard | 100.028.374 | |
| PubChem | 4873 | |
| Arzneistoffangaben | ||
| ATC-Code |
| |
| Eigenschaften | ||
| Molare Masse | 74,55 g/mol | |
| Aggregatzustand | fest | |
| Dichte | 1,98 g/cm3 | |
| Schmelzpunkt | 773 °C | |
| Siedepunkt | 1413 °C | |
| Dampfdruck | 10 Pa (700 °C) | |
| Löslichkeit | ||
| Brechungsindex | 1,4902 | |
Kaliumchlorid (KCl), das Kaliumsalz der Salzsäure, bildet farblose, salzig-bitter schmeckende, wasserlösliche Kristalle mit einem Schmelzpunkt von 773 °C und einer Dichte von 1,98 g/cm3. Es löst sich bei 20 °C zu 347 g/l in Wasser. Als Mineral heißt es Sylvin.

Weltweit gibt es zahlreiche kaliumchloridhaltige Salzvorkommen. Von herausragender Bedeutung sind die Vorkommen in Kanada, in der GUS und Deutschland. Bis 2014 wurde das über 240 Millionen Tonnen große Vorkommen in der Wüste Lop Nor im Seebecken von Lop Nor in VR China mit der weltgrößten Produktionsstätte für 3 Millionen Tonnen Dünger erschlossen.
In der Natur kommt Kaliumchlorid als Sylvin (Sylvit) vor. Weitere weit verbreitete kalium- und chloridhaltige Minerale und Gesteine sind Carnallit – KCl · MgCl2 · 6 H2O, Kainit – KCl · MgSO4 · 3 H2O und Sylvinit – KCl · NaCl.
Gewinnung
Das Verfahren des Auskristallisierens des schwerer löslichen Kaliumchlorids beim Eindampfen von konzentrierten wässrigen Lösungen von Carnallit (KMgCl3 · 6 H2O) hat technisch die größte Bedeutung. Auch durch Flotation von kaliumchloridhaltigen Salzgemengen, zum Beispiel im Kalibergbau gewonnener Rohsalze, kann Kaliumchlorid gewonnen werden. Eine weitere Möglichkeit besteht im Heißlöseverfahren, welches ein selektives Herauslösen des KCl aus Salzgemengen auf Grund unterschiedlicher Temperaturabhängigkeiten der Löslichkeiten von Salzen erlaubt. Im ESTA-Verfahren gelingt die Gewinnung durch elektrostatische Trennung aus Salzgemengen. Durch Neutralisation von Salzsäure und Kalilauge gemäß der Gleichung
gelingt die Darstellung.
Verwendung
Kaliumchlorid wird in der Lebensmitteltechnik als Festigungsmittel und Geschmacksverstärker eingesetzt. Es ist in der Europäische Union als Lebensmittelzusatzstoff der Nummer E 508 ohne Höchstmengenbeschränkung (quantum satis) für alle als Zusatzstoff zugelassenen Lebensmittel erlaubt. Zudem findet es Verwendung als Bestandteil künstlicher Speisesalze, z.B. Pansalz, zur Einsparung von Natriumchlorid.
Kaliumchlorid wird großtechnisch zur Herstellung von Kalidünger genutzt. Des Weiteren ist Kaliumchlorid der Rohstoff für die Herstellung fast aller technisch genutzten Kaliumverbindungen wie beispielsweise Kaliumcarbonat, Kaliumhydroxid und auch der Legierung NaK.
Die Metallindustrie nutzt Kaliumchlorid als Härtesalz, die Emailleindustrie als Schwebemittel. In der Erdölindustrie dient es zur Stimulation von Lagerstätten. Als Streusalz ist es wegen der tieferen Schmelztemperatur einer Kaliumchlorid-Wasser-Mischung auch bei Temperaturen unter −10 °C wirtschaftlich einsetzbar.
Kaliumchlorid ist ein Bestandteil künstlich hergestellter isotonischer Lösungen, einer Lösung mit gleichem osmotischem Druck wie das menschliche Blut. Auch in schmerzhemmenden Zahncremes für schmerzempfindliche Zähne ist es enthalten. Im Labor wird es zu Elektrolyt- und Aufbewahrungslösung für pH-Messelektroden und Redox-Elektroden (annähernd gesättigt mit 3 mol/l KCl-Lösung) genutzt. Durch die gleiche Ionenbeweglichkeit von Kalium- und Chloridionen ist diese Lösung potentialneutral. Es dient auch als Kalibrierstandard für Betastrahlung. Kalium enthält zu 0,0118 % das Isotop 40K, dieses liefert 16350 Bq pro Kilogramm KCl, davon sind 89,28 % Betastrahlung und 10,72 % Gammastrahlung mit 1,46083 MeV.
Beim Hydraulic Fracturing wird es meistens mit Wasser, Sand und anderen Chemikalien in die Erde gepumpt um die Gesteinsschichten aufzubrechen.
Toxikologie
Die Injektion von hohen Dosen Kaliumchlorid kann zum Herzstillstand durch Hyperkaliämie führen. Das wird beim Einschläfern von Tieren, bei der Hinrichtung durch die Giftspritze und zur Verhinderung von Lebendgeburten bei späten Schwangerschaftsabbrüchen ausgenutzt. Verwendet wird es ebenfalls für kardioplegische Lösungen (Blutkardioplegie nach Calafiore) zum Einleiten des Herzstillstands bei Operationen mit Herz-Lungen-Maschinen.
Nachweis
Der klassische Nachweis des Cl−-Ions gelingt durch Fällung mit Ag+, Pb2+ oder Hg22+ als Silberchlorid AgCl, Blei(II)-chlorid PbCl2 sowie als Quecksilber(I)-chlorid Hg2Cl2. Der Nachweis des K+-Ions ist über die violette Flammenfärbung beziehungsweise Fällung als Kaliumperchlorat (KClO4) möglich. Mit Natriumtetraphenylborat kann ebenfalls ein schwerlösliches Kaliumsalz gefällt werden.
Spektroskopisch gelingt der Nachweis der Elemente zum Beispiel mittels Atomabsorptionsspektroskopie. Als Gift im menschlichen Körper gehört Kaliumchlorid zu den am schwersten nachzuweisenden Giften, die derzeit bekannt sind.
Toxikologie und Forensik
Rechtsmedizinisch kann eine Vergiftung mit Kaliumchlorid nur schwer nachgewiesen werden. Der natürliche Spiegel steigt nach dem Tod durch Zellzerfall und damit Übertritt des intrazellulären Kaliums in alle anderen Kompartimente, schnell an. Gelingt der Nachweis einer Vergiftung, muss ein ärztlicher Behandlungsfehler durch
- Überdosierung einer oralen Kaliumgabe oder Einnahme von Kalium-steigernden Medikamenten (Spironolacton, ACE-Hemmer etc.) im Rahmen einer Niereninsuffizienz,
- Überdosierung im Rahmen einer intravenösen Gabe,
- versehentliche Fehlinfusion
von der bewussten Verabreichung abgegrenzt werden.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 11.10. 2025