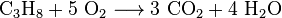GHS-Gefahrstoffkennzeichnung
aus Verordnung (EG) Nr. 1272/2008 (CLP), ggf. erweitert
| |||
| H- und P-Sätze | H:
| ||
P:
| |||
| Sicherheitshinweise | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| MAK | DFG/Schweiz: 1000 ml/m3 bzw. 1800 mg/m3 | |||||||
Propan ist ein farbloses brennbares Gas und gehört zu den Kohlenwasserstoffen. Es steht in der homologen Reihe der Alkane an dritter Stelle.
Propan ist ein farb- und geruchloses Gas, hat einen Schmelzpunkt von −187,7 °C und einen Siedepunkt von −42 °C. Die kritische Temperatur liegt bei 96,8 °C, der kritische Druck bei 4,2 MPa und die kritische Dichte bei 0,22 g/cm3. Propan kann leicht verflüssigt werden. Es löst sich bei 20 °C zu 75 mg/l in Wasser.
Propan ist schwerer als Luft und wirkt in hohen Konzentrationen narkotisierend bis erstickend.
Propan ist hochentzündlich und bildet zwischen einem Volumenanteil von 2,12 % bis 9,35 % in Luft explosionsfähige Gemische. Seine Zündtemperatur liegt bei 470 °C (nach DIN 51794). Der Heizwert beträgt 93 MJ/m3.
| Strukturformel | ||
|---|---|---|
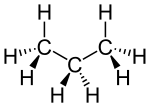 | ||
| Keile zur Verdeutlichung der Geometrie | ||
| Allgemeines | ||
| Name | Propan | |
| Andere Namen | R290 | |
| Summenformel | C3H8 | |
| CAS-Nummer | ||
| EG-Nummer | 200-827-9 | |
| ECHA-InfoCard | ||
| PubChem | ||
| ChemSpider | ||
| Kurzbeschreibung | farb- und geruchloses Gas | |
| Eigenschaften | ||
| Molare Masse | 44,10 g/mol | |
| Aggregatzustand | gasförmig | |
| Dichte |
| |
| Schmelzpunkt | −188 °C | |
| Siedepunkt | −42 °C | |
| Dampfdruck | 0,83 MPa (20 °C) | |
| Löslichkeit | praktisch unlöslich in Wasser (75 mg/l bei 20 °C) | |
| Dipolmoment | 0,084 D (2,8 · 10−31 C · m) | |
| Thermodynamische Eigenschaften | ||
| ΔHf0 | −103,8 kJ/mol | |
Propan ist ein natürlich vorkommendes Gas. Es entsteht zusammen mit anderen Kohlenwasserstoffen wie Erdöl und Butan durch die Zersetzung und Reaktion organischer Stoffe innerhalb geologischer Zeiträume. Propan wird aus Erdölfeldern freigesetzt, indem es von anderen Kohlenwasserstoffen getrennt und für den kommerziellen Gebrauch raffiniert wird. Industriell wird Propan bei der Förderung von Erdgas als Nebenprodukt gewonnen und in einer Erdölraffinerie beim Cracken von Erdöl hergestellt.
Im Labor kann Propan durch eine Additionsreaktion von Propen mit Wasserstoffsynthetisiert werden:
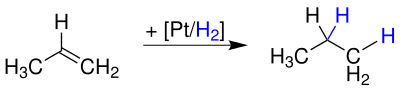
Damit die Additionsreaktion ablaufen kann, werden z. B. Platin-, oder Palladiumkatalysatorenverwendet.

Es wird verflüssigt als Brenn- und Heizgas eingesetzt (Flüssiggas), z.B. bei Pkw als Autogas, für den Heißluftballon, in Feuerungsanlagen, beim Kochen, für Warmwasserbereiter in Gasgrills oder bei Außenbordmotoren als Brennstoff.
Als Kältemittel hat es die Bezeichnung R290 und wird in Kühlgeräten und Wärmepumpen eingesetzt. In Australien wird Propan schon in über 1.000.000 Auto-Klimaanlagen eingesetzt. Propan hat ein niedriges Treibhauspotenzial (das 3,3-fache des der gleichen Menge Kohlendioxid), kein Ozonabbaupotential und kann als Ersatz für R12 , R22 , R134a und andere Fluorchlorkohlenwasserstoffe dienen. Alte Anlagen dürfen aber nicht einfach mit Propan gefüllt werden, da es brennbar ist. Für Propananlagen sind eigene Sicherheitsvorschriften zu erfüllen.
Propan ist möglicher Bestandteil des Treibgases in Sprühdosen (Lebensmittelzusatzstoff E 944) und Softairs sowie zur Herstellung von Ethylen und Propen. Gasgemische von z.B. 40 % Propan und 60 % Butan werden für technische Geräte wie Löt- und Schweißgeräte, Gas-Rechauds, Feuerzeuge usw. verwendet.
Propan wird unter Druck verflüssigt in Gasflaschen oder Tanks gelagert.
Weiterhin wird es auch in unterirdischen Kavernen gelagert. Das Einlagern geschieht vorzugsweise in den verbrauchsarmen Monaten, um Verbrauchsspitzen im Winter abdecken zu können.
Propan verbrennt zu Kohlenstoffdioxid (CO2) und Wasser (H2O):