
Capronsäure
| Sicherheitshinweise | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| Toxikologische Daten | |||||||
Capronsäure (n-Hexansäure) ist eine gesättigte Fett- bzw. Carbonsäure, die sich vom n-Hexan ableitet. Der Name leitet sich wie bei der Caprylsäure und der Caprinsäure vom Lateinischen capra für Ziege ab, was ebenso wie der historische Trivialname „Ziegensäure“ auf den charakteristischen Geruch der Säure hinweist. Ihre Salze und Ester heißen Capronate bzw. Hexanoate. In der Nomenklatur der Fettsäuren hat sie die Bezeichnung 6:0.
| Strukturformel | ||
|---|---|---|
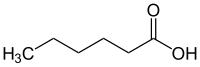
| ||
| Allgemeines | ||
| Name | Capronsäure | |
| Andere Namen | ||
| Summenformel | C6H12O2 | |
| Kurzbeschreibung | ölige, farblose bis schwachgelbe Flüssigkeit mit stechendem schweißartigem Geruch nach Ziege[5][6] | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | 142-62-1 | |
| EG-Nummer | 205-550-7 | |
| ECHA-InfoCard | 100.005.046 | |
| PubChem | 8892 | |
| Eigenschaften | ||
| Molare Masse | 116,16 g/mol | |
| Aggregatzustand | flüssig[5] | |
| Dichte | 0,9212 g/cm3 (25 °C)[7] | |
| Schmelzpunkt | −4 °C[5] | |
| Siedepunkt | 206 °C[5] | |
| Dampfdruck | 5,8 Pa (20 °C)[5] | |
| pKS-Wert | 4,85 (25 °C)[8] | |
| Löslichkeit |
| |
| Brechungsindex | 1,4163 (20 °C)[7] | |
Vorkommen

Sie kommt chemisch gebunden zu 2–3 Prozent in Triglyceriden des Milchfetts in der Milch sowie auch im Kokosöl vor. Daneben kommt sie verestert in verschiedenen Samenölen und ätherischen Ölen; Fichtennadelöle, Lavendelöl, Zitronengrasöl und auch in Früchten z. B. Erdbeere, Himbeere, sowie in Bier und Kaffee vor.[10][11][12] Capronsäure dient, wie viele andere Carbonsäuren, zur Synthese von Fruchtaromen durch Veresterung.
Eigenschaften
Capronsäure ist eine bei Zimmertemperatur farblose, ölige, übelriechende Flüssigkeit, die in Wasser schwer löslich ist. Die brennbare Substanz hat einen Flammpunkt von 102,5 °C.[5]
Einzelnachweise
- ↑ Chevreul: Ueber die Ursachen der Verschiedenheit der Seife hinsichtlich auf Härte, Weiche und Geruch, und über eine neue Gruppe organischer Säuren. In: Polytechnisches Journal. 11, 1823, S. 428.
- ↑ Rudolph Böttger: Tabellarische Uebersicht der specifischen Gewichte der Körper. 1837, S. 26 (Volltext/Vorschau in der Google-Buchsuche).
- ↑ Otto Ule, Karl Müller: Die Natur: Zeitung zur Verbreitung naturwissenschaftlicher Kenntnis... Band 8, Halle, 1859, S. 171, eingeschränkte Vorschau in der Google-Buchsuche.
- ↑ Eintrag zu CAPROIC ACID in der CosIng-Datenbank der EU-Kommission.
- ↑ Hochspringen nach: a b c d e f g h i j k Eintrag zu Capronsäure in der GESTIS-Stoffdatenbank des Institut für Arbeitsschutz der Deutschen Gesetzlichen Unfallversicherung. (JavaScript erforderlich)
- ↑ Hochspringen nach: a b Eintrag zu Hexansäure. In: Römpp Online. Georg Thieme Verlag.
- ↑ Hochspringen nach: a b W. M. Haynes (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-298.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Dissociation Constants of Organic Acids and Bases, S. 8-46.
- ↑ Claudia Synowietz (Hrsg.): Taschenbuch für Chemiker und Physiker. Begründet von Jean d’Ans, Ellen Lax. 4. Auflage. Band 2: Organische Verbindungen. Springer, Berlin 1983, ISBN 3-540-12263-X.
- ↑ Walter Karrer: Konstitution und Vorkommen der organischen Pflanzenstoffe. Springer, 1958, ISBN 978-3-0348-6808-2 (Reprint), S. 289.
- ↑ Hexanoic acid bei PlantFA Database. (Michigan State University)
- ↑ J. Schormüller: Die Bestandteile der Lebensmittel. Springer, 1965, ISBN 978-3-642-46012-8, S. 768.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 17.02. 2026
