
Tritium
| Sicherheitshinweise | |||
|---|---|---|---|

Radioaktiv | |||
|
Tritium (ˈtʁiːt͡si̯ʊm, von altgriechisch τρίτος trítos ‚der Dritte‘), auch 3H, überschwerer Wasserstoff oder superschwerer Wasserstoff ist ein in der Natur in Spuren vorkommendes Isotop des Wasserstoffs. Sein auch Triton genannter Atomkern besteht aus einem Proton und zwei Neutronen. Tritium ist ein radioaktiver Betastrahler. Es zerfällt mit einer Halbwertszeit von 12,32 Jahren zu stabilem Helium-3 (3He).
Namensgebung
|
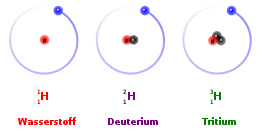
Aufgrund der großen Bedeutung der Wasserstoffisotope und weil sich ihre Massen stark unterscheiden, hat man den Isotopen nicht nur eigene Namen gegeben, sondern den Isotopen Deuterium und Tritium auch eigene Elementsymbole: Für 2H kann man auch D schreiben, und für 3H auch T. In diesem Fall steht H dann speziell für 1H.
| Strukturformel | ||
|---|---|---|
| Allgemeines | ||
| Name | Tritium | |
| Andere Namen |
| |
| Summenformel | T2 (molekulare Form) | |
| Kurzbeschreibung | farbloses Gas | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer |
|
|
| EG-Nummer | 233-070-8 | |
| ECHA-InfoCard |
| |
| PubChem | ||
| Eigenschaften | ||
| Molare Masse | ||
| Aggregatzustand | gasförmig | |
| Schmelzpunkt | ||
| Siedepunkt | 25,05 K (−248,1 °C) | |
| Dampfdruck | 215,98 hPa (am Schmelzpunkt) | |
Andere Elemente haben für Isotope keine eigenen Namen und Symbole, da dort das Massenverhältnis zwischen den Isotopen weit geringer ist. Am größten ist es mit 1 : 1,3271 noch bei dem Isotopenpaar 3He und 4He, das aber chemisch inert ist. Bei Kohlenstoff ist das Verhältnis dann schon auf 1 : 1,0836 für 12C und 13C gefallen.
Geschichte
Als Entdecker gelten Ernest Rutherford, Mark Oliphant und Paul Harteck (1934), die es aus Deuterium erzeugten. Der Nachweis über einen magnetooptischen Effekt (Allison-Effekt) durch Wendell Latimer 1933 geriet in den Hintergrund, nachdem dieser Effekt noch im selben Jahr in Misskredit geriet. Isoliert wurde es 1939 zuerst von Luis W. Alvarez und Robert Cornog, die auch dessen Radioaktivität erkannten. Willard Libby erkannte in den 1950er Jahren, dass man Tritium für radiometrische Datierungen von Wasser und Wein benutzen konnte.
Entstehung
Natürliche Herkunft
Tritium entsteht auf natürliche Weise vor allem in der Stratosphäre. Schnelle Protonen der kosmischen Strahlung bilden durch Spallation teilweise direkt Tritium, vor allem aber sekundäre Neutronen, die in der Stratosphäre und oberen Troposphäre in Reaktionen mit Stickstoff Tritium bilden:
kurz:
oder:
Tritium bildet zunächst HT (Tritiumwasserstoff), diffundiert (sofern in der Stratosphäre entstanden) zur Tropopause, oxidiert in der Troposphäre mit einer Zeitkonstanten von 6,5 Jahren durch photochemische Reaktionen zu HTO (T-haltiges Wasser) und regnet dann vergleichsweise schnell aus. Aus Bildung und radioaktivem Zerfall stellt sich ein Fließgleichgewicht ein, wodurch sich in der Biosphäre ständig ca. 3,5 kg Tritium aus natürlicher Produktion befinden, zu 99 % in oberflächennahen Schichten der Ozeane.
Nebenprodukt der Kernspaltung
In mit schwerem Wasser moderierten Reaktoren fällt Tritium in einer Menge von rund 1 kg pro 5 GWa (Gigawattjahre) – das sind etwa 150 Peta-Joule erzeugter elektrischer Energie – als unvermeidliches Nebenprodukt an. Die Extraktion aus dem Kühlwasser ist aufwändig, da hierzu eine Isotopentrennung erforderlich ist. Einige – aber nicht alle – Schwerwasserreaktoren extrahieren dennoch Tritium aus dem Kühlwasser zum Verkauf auf dem freien Markt oder Einsatz in staatlichen Projekten.
Auch im Kühlmittel des Primärkreises vieler Druckwasserreaktoren bildet sich Tritium, da dem Wasser eine gewisse Menge an Borsäure zur Steuerung der Reaktivität im Reaktorkern beigesetzt wird. Die erwünschte Reaktion ist dabei, dass Bor-10 ein Neutron absorbiert, und dann sofort in ein Alpha-Teilchen und Lithium-7 zerfällt. Eine unerwünschte Nebenreaktion ist jedoch, dass Bor-11 ein Neutron absorbiert und dann in Tritium und Beryllium-9 zerfällt.
Tritium ist außerdem ein weniger häufiges Nebenprodukt bei der Kernspaltung von spaltbaren Atomkernen wie 235U, 239Pu oder 233U und entsteht dabei mit einer Häufigkeit von ungefähr 1 Tritiumkern pro 104 Spaltungen. Das Tritium entsteht bei 7 % der ternären Zerfälle, also wenn das Ausgangsnuklid in drei anstatt zwei Bruchstücke gespalten wird. In der Regel verbleibt dieses Tritium zusammen mit den anderen Spaltprodukten in den Brennelementen. Bei einem Unfall mit Kernschmelze oder bei der Wiederaufarbeitung von Kernbrennstoffen kann es aber freigesetzt werden. Eine Gewinnung von Tritium aus abgebrannten Kernbrennstoff ist zwar denkbar, wird jedoch derzeit nicht praktiziert. Bei nasschemischen Verfahren wie PUREX werden verwendete Prozessflüssigkeiten (darunter hauptsächlich Wasser) entsprechend kontaminiert, weswegen inzwischen großer Wert auf Rückgewinnung dieser Flüssigkeiten gelegt wird.
Produktion aus Lithium
Tritium kann durch Reaktion von 6Li mit Neutronen hergestellt werden:
In Wasserstoffbomben wird das zur Fusion nötige Tritium überwiegend erst während der Explosion der Bombe auf diesem Weg hergestellt. Die dazu benötigten Neutronen stammen anfangs aus der Spaltung von Uran oder Plutonium, später auch aus der Fusionsreaktion selbst.
Für Kernfusionsreaktoren ist die Produktion von Tritium aus Lithium auf demselben Weg vorgesehen: Anfangs, insbesondere für den Betrieb von Forschungsreaktoren, soll Tritium mittels des Neutronenflusses in Kernreaktoren erbrütet werden. Später soll das nötige Tritium im Blanket der Kernfusionsreaktoren hergestellt werden.
Eigenschaften
Radioaktivität
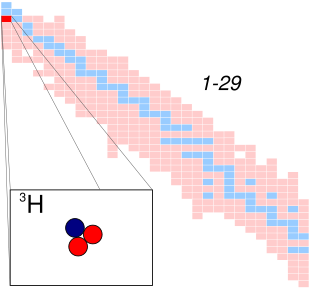
Während sich im Atomkern des Wasserstoffatoms (1H) neben dem Proton kein Neutron befindet und im Deuterium (2H oder D) ein Neutron, sind es im Tritium zwei. Im Gegensatz zu 1H und 2H ist der Tritiumkern instabil und zerfällt mit einer Halbwertszeit von 12,32 Jahren unter Emission eines Elektrons und eines Antineutrinos in das Heliumisotop 3He (Beta-Minus-Zerfall):
Bei diesem Zerfall wird insgesamt eine Energie von etwa 18,6 keV frei:
.
Davon erhält das Elektron im Mittel 5,7 keV kinetische Energie. Im Vergleich zu anderen Betastrahlern ist die Strahlung sehr weich. In Wasser wird sie nach wenigen Mikrometern gestoppt; sie kann auch die oberen Hautschichten nicht durchdringen. Die Radioaktivität von Tritium ist daher vor allem beim Verschlucken oder beim Einatmen gefährlich.
Weitere Eigenschaften
Das Symbol ist 3H; aus Gründen der Vereinfachung in der Formelschreibweise wird häufig auch T verwendet.
Tritiumoxid (überschweres Wasser) T2O hat eine Siedetemperatur von 101,51 °C und eine Schmelztemperatur von 4,48 °C.
Verwendung
Unter anderem in der Biologie, Chemie und Medizin wird Tritium als sogenannter Tracer zur Markierung bestimmter Substanzen verwendet, auch zur Altersbestimmung von Grundwasser.
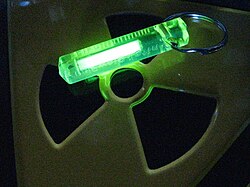
In Tritiumgaslichtquellen (langlebige Leuchtmittel) wird gasförmiges Tritium zusammen mit einem Leuchtstoff in versiegelten Röhrchen aus Borosilikatglas verwendet. Die Betastrahlung des Tritiums regt die Leuchtstoff-Beschichtung innen auf dem Glasröhrchen zu einem schwachen Leuchten (Fluoreszenz) an. Diese »kalten Leuchten« haben eine theoretische Lebensdauer von mehreren Jahrzehnten und sind in verschiedenen Farben verfügbar.
Die vorgenannten Tritiumgaslichtquellen kommen auch als Lichtquelle auf Uhrenzifferblättern und -zeigern bestimmter Uhrenmodelle zur Anwendung. In Kompassen, wie sie die US Army in den 1980er Jahren benutzte, verwendete man entsprechend 120 mCi (4,4 GBq) Tritium in der Farbe für Markierungen der Himmelsrichtungen. Auch auf Visiere von Waffen wurde tritiumhaltige Leuchtfarbe aufgebracht.
Ionisationsrauchmelder arbeiten teilweise mit einer Tritiumgas-Ampulle als Ionisator. Bei der Herstellung und Lagerung größerer Mengen bestehen wegen der Radioaktivität allerdings gesundheitliche Risiken. Daher wird es durch phosphoreszierende Leuchtmittel, wie z.B. Superluminova ersetzt. In Rauchmeldern kann statt Tritium auch 241Am (Americium) verwendet werden.
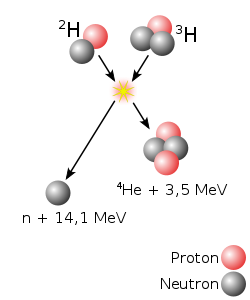
Ein 1:1-Gemisch von Deuterium und Tritium (D-T) hat die günstigsten Eigenschaften als Brennstoff für die Fusionsenergie: Eine hohe Energieausbeute, einen relativ großen Wirkungsquerschnitt, die kleinstmögliche dafür zu überwindende Coulombkraft (nur eine elektrische Ladung je Atom) und dadurch eine vergleichsweise niedrige Fusionstemperatur. Sie beträgt in Fusionsreaktoren etwa 100 Millionen Kelvin, gegenüber 400 Millionen Kelvin bei der in dieser Hinsicht nächstgeeigneten Deuterium-Deuterium-Reaktion. Deshalb kommt für zukünftige Fusionskraftwerke nur ein D-T-Gemisch in Betracht. Für deren Dauerbetrieb wären jedoch ausreichende Mengen Tritium nur durch Erbrüten aus Lithium-6 im Reaktor selbst herstellbar. Erste Experimente, bei denen D-T-Fusionen nachgewiesen wurden, fanden bisher an den Test-Anlagen Joint European Torus (JET) in Culham, England sowie am Tokamak Fusion Test Reactor (TFTR) in Princeton statt. D-T-Experimente in größerem Maßstab sind für die zweite Experimentphase des Projekts ITER vorgesehen. Anlagen zur Erforschung der Grundlagen eines Fusionskraftwerks wie etwa in Deutschland der Tokamak ASDEX Upgrade in Garching oder der Stellarator Wendelstein 7-X in Greifswald verwenden dagegen nur Deuterium- oder Wasserstoff-Plasmen, weil es erst einmal nur darum ging und geht, ein stabiles Plasma zu erzeugen. Damit besteht unmittelbar nach jedem Experiment Zugang zu der Anlage und den Messgeräten und der Strahlenschutz-Aufwand kann geringer gehalten werden (der ist auch bei einem Deuterium-Plasma notwendig, weil darin auch bei 100 Millionen Kelvin schon zahlreiche Deuterium-Deuterium-Fusionen stattfinden).
Tritium ist auch ein wesentlicher Bestandteil bestimmter Kernwaffen. Bereits wenige Gramm eines gasförmigen Deuterium-Tritium-Gemischs können in Kernspaltungs-Waffen deren Sprengstoffwirkung um den Faktor 2 verstärken, auch „boosting“ genannt. Für Neutronenbomben ist Tritium sogar essentiell zur Funktion notwendig; hier werden bis zu 20 Gramm Tritium pro Sprengkopf benötigt. In Wasserstoffbomben wird Tritium nur als Booster und zur Einstellung der Sprengkraft in der Fissionstufe verwendet, in der Fusionstufe kommt hingegen Lithiumdeuterid zum Einsatz, aus dem erst unter Neutronenbeschuss Tritium gebildet wird.
Wegen seiner relativ kurzen Halbwertzeit von 12,3 Jahren wird Tritium zur Altersbestimmung von oberflächennahem Grundwasser oder zur Untersuchung von hydrologischen Fließbedingungen verwendet. Ausgangspunkt der Berechnungen ist der Eintrag des Tritium in den 1950er- und frühen 1960er-Jahren in das Grundwasser. Ursachen des Eintrags waren die zahlreichen Atomtests in der Atmosphäre, die erhebliche Mengen an Tritium freisetzten.
Durch Betazerfall von Tritium entsteht nichtradioaktives Helium-3. Auf Grund seiner extremen Seltenheit in natürlichen Heliumquellen stellt dies derzeit die am wenigsten preisintensive Quelle für Helium-3 dar. Es wird in der Grundlagenforschung benötigt.
Sicherheitshinweise
Die von Tritium ausgehenden chemischen Gefahren sind zwar mit denen von Wasserstoff identisch, aber vergleichsweise zu vernachlässigen gegenüber den radioaktiven Gefahren als gasförmiger Betastrahler, die auch völlig andere Handhabungsvorschriften erfordern. Die Kennzeichnung für Wasserstoff gemäß Anhang VI der Verordnung (EG) Nr. 1272/2008 (CLP), die sich nur mit den von der Chemie ausgehenden Gefahren befassen, würden hier eher verharmlosend wirken und wurden deshalb weggelassen, zumal Tritium nur in dafür fachlich qualifizierten Laboratorien und nur in geringen Mengen gehandhabt wird.
Tritium ist nicht stark radiotoxisch, kann jedoch in Form von Wasser im Körper gespeichert und umgesetzt werden. Eine französisch-belgische Studie von 2008 kommt zum Schluss, dass seine radiologischen Wirkungen bisher unterschätzt wurden: Es kann sich z.B. in die DNS (Erbsubstanz) einlagern, was vor allem bei einer Schwangerschaft problematisch sein kann.
Tritium kann als Isotop des Wasserstoffs überall am Stoffwechsel mitwirken, wo sonst Wasserstoff vorkommt. Im Unterschied zu Isotopen, welche sich spezifisch in gewissen Zielgeweben anreichern, verteilt sich Tritium im ganzen Körper. Im menschlichen Stoffwechsel wird elementarer Wasserstoff aber nicht gebraucht, somit wird reines, gasförmiges Tritium, wenn es aufgenommen wird, nur zu einem sehr kleinen Teil im Blut gelöst. Der größte Teil wird wieder als Gas abgeatmet. Wird hingegen Tritium als Teil eines Wassermoleküls aufgenommen, so wird es sich relativ schnell mit dem schon im Körper vorhandenen Wasser vermischen. Somit ist – laut dem Schweizer Nuklearsicherheitsinspektorat ENSI – die Aufnahme von Tritiumatome enthaltenden Wassermolekülen (Tritiumoxid) wesentlich gefährlicher als diejenige von gasförmigem Tritium. In den Urin gelangt aufgenommenes Wasser mit einer Halbwertszeit von etwa 10 Tagen. Generell kann gesagt werden, dass sich Tritium überall dort „in den Stoffwechsel einmischen“ kann, wo eigentlich Wasserstoff gebraucht würde. Im Bereich von kleinen Dosen können Mutationen oder die Entstehung von Krebs die Folge sein, wobei sich deren Wahrscheinlichkeit mit der Dosis erhöht. Bei höheren Dosen überwiegen akute Effekte.
Nachweis
Der Nachweis von Tritium erfolgt unter anderem anhand der Wirkungen der Radioaktivität mittels Flüssigszintillationszählern oder offenen Ionisationskammern. Ebenso können Massenspektrometer zum Nachweis verwendet werden.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 03.07. 2024