
cis-trans-Isomerie
Die cis-trans-Isomerie oder (Z)-(E)-Isomerie bezeichnet in der Chemie eine spezielle Form der Konfigurationsisomerie, bei der sich die Moleküle nur hinsichtlich der relativen Stellung von zwei Substituenten bezüglich einer Referenzebene unterscheiden. Falls es mehr als zwei Substituenten gibt, betrachtet man jene beiden, welche nach der Cahn-Ingold-Prelog-Konvention die höchste Priorität besitzen.
- Von einer cis- bzw. (Z)-Anordnung spricht man, wenn sich beide Substituenten auf der gleichen Seite der Referenzebene (zusammen) befinden.
- Von einer trans- bzw. (E)-Anordnung spricht man, wenn sich die zwei Substituenten auf entgegengesetzten Seiten der Referenzebene (entgegen) befinden.
Eine Referenzebene kann beispielsweise eine Doppelbindung oder ein Ringsystem sein. cis- und trans-Isomere unterscheiden sich in den chemischen und physikalischen Eigenschaften wie zum Beispiel Schmelztemperatur, Siedetemperatur, Bindungsenthalpie. cis- und trans- bzw. (Z)- und (E)- selbst werden als Deskriptoren bezeichnet und dem systematischen Substanznamen vorangestellt.
cis-trans-Isomerie bei Doppelbindungen
cis-trans-Isomerie tritt auf, wenn beide Atome einer Doppelbindung unterschiedliche Substituenten tragen:
- Wenn beide Substituenten auf der gleichen Seite liegen, spricht man von einem cis- oder (Z)-Isomer.
- Wenn die beiden Substituenten auf entgegengesetzten Seiten der Doppelbindung liegen, spricht man von einem trans- oder (E)-Isomer.
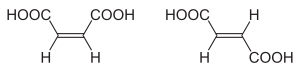
Ein Beispiel für (Z)-(E)-Isomerie ist das Isomerenpaar (Z)-Butendisäure (Maleinsäure) und (E)-Butendisäure (Fumarsäure).
Sind an den beiden Kohlenstoffatomen einer Doppelbindung jeweils ein Wasserstoffatom und ein größerer Substituent gebunden (vicinale Doppelbindungen), ist die Zuordnung von cis und trans eindeutig und diese traditionellen Nomenklaturbezeichnungen können verwendet werden. Sind dagegen mehr Substituenten vorhanden, muss die (E/Z)-Nomenklatur verwendet werden, für die über die Sequenzregel eine eindeutige Prioritäten-Reihenfolge festgelegt wurde.
cis-trans-Isomerie bei Ringsystemen
cis-trans-Isomerie gibt es auch bei cyclischen Verbindungen, etwa bei Monocyclen, die an verschiedenen Kohlenstoffatomen Substituenten tragen, oder bei Bicyclen. Zur Benennung von Ringsystemen nach IUPAC-Regeln werden die Vorsilben „cis-“ und „trans-“ dem Verbindungsnamen kursiv vorangestellt und zur alphabetischen Einordnung nur bei Namensgleichheit herangezogen.
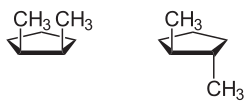
Ein Beispiel für eine monocyclische Verbindung mit cis-trans-Isomerie ist 1,2-Dimethylcyclopentan: Die beiden Methyl-Substituenten können sich entweder auf der gleichen Seite der Molekülebene befinden (cis-Form) oder auf einander entgegengesetzten Seiten (trans-Form).
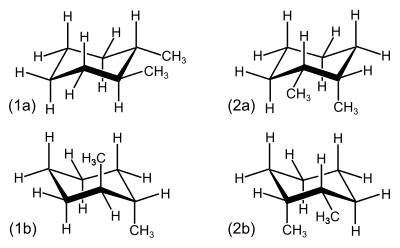
Bei 6-Ringen wie bei 1,2-Dimethylcyclohexan lassen sich die cis- und trans-Isomere schwer erkennen, da die Verbindungen nicht als planare Ringe betrachtet werden sollten. Verbindungen dieser Art liegen meist in der energetisch bevorzugten Sesselkonformation vor. Da je zwei Sesselkonformationen durch Ringinversion vorliegen, lassen sich beispielsweise trans-1,2-Dimethylcyclohexan und cis-1,2-Dimethylcyclohexan nicht unmittelbar erkennen. Bei trans-1,2-Dimethylcyclohexan liegen beide Methylgruppen entweder äquatorial oder axial vor. In den cis-Formen liegen je eine Methylgruppe äquatorial, die andere axial vor.
 |
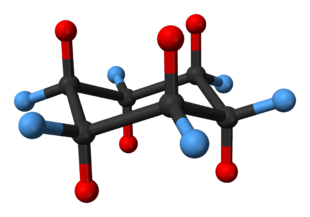 |
| (1a) und (1b) Sessel-Konformationen von trans-1,2-Dimethylcyclohexan; (2a) und (2b) Sessel-Konformationen von cis-1,2-Dimethylcyclohexan. | Stellungen bei der Sesselkonformation von Cyclohexan. Die Wasserstoffatome in axialer Stellung sind rot markiert und zueinander trans-positioniert. Die Wasserstoffatome in äquatorialer Stellung sind blau markiert und stehen zueinander ebenfalls in trans-Position, was aber schwerer zu erkennen ist. |
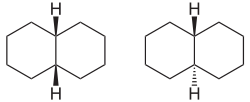
Ein Beispiel für eine bicyclische Verbindung ist Decalin, da die beiden Sechserringe unterschiedlich verknüpft sein können: Die beiden Wasserstoffatome an den Verknüpfungsstellen können sich entweder auf der gleichen Seite des Decalinmoleküls befinden (cis-Form) oder auf einander entgegengesetzten Seiten (trans-Form).
Gegenseitige Umwandlung
 |
| Durch eine Peptidyl-Prolyl-cis-trans-Isomerase (PPIase) katalysiertes Gleichgewicht: Ohne enzymatische Katalyse findet die Rotation um die blau markierte Bindungsachse der Peptidbindung zwischen dem N-Terminus von L-Prolin und dem C-Terminus einer anderen Aminosäure nur langsam statt. |
Bei einer Doppelbindung lassen sich die cis- und trans-Isomere ineinander umwandeln (cis-trans-Interkonversion). Hierzu ist eine vorübergehende Auflösung der π-Bindung nötig, was meist nur bei hohen Temperaturen oder unter Strahlungseinfluss vonstattengeht. Solche Umwandlungen sind z. B. ein zentraler Bestandteil des Sehvorganges (siehe Retinal).
Die zwischen dem N-Terminus von L-Prolin und dem C-Terminus einer anderen Aminosäure in Peptiden vorliegende Amidbindung (Peptidbindung) kann sowohl in der trans- als auch in der cis-Konfiguration vorliegen, da diese Bindung einen gewissen Doppelbindungscharakter aufweist. Ein Wechsel zwischen beiden Konfigurationen findet nur langsam statt, kann jedoch enzymatisch durch eine Peptidyl-Prolyl-cis-trans-Isomerase katalysiert werden.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 29.03. 2024