
Tocopherole
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| Toxikologische Daten |
| ||||||||
Tocopherole ist ein Sammelbegriff für verschiedene fettlösliche Substanzen, die einen modifizierten Chromanring mit einer gesättigten Seitenkette haben. Hiervon weisen die (RRR)-Stereoisomere eine biologische, antioxidative Aktivität auf und werden dann dem Vitamin E zugeordnet. Häufig wird der Begriff Vitamin E allein für (RRR)-α-Tocopherol, die am besten erforschte Form von Vitamin E, verwendet. Ferner gibt es noch MDT (marine derived tocopherols).
Der Name leitet sich vom altgriechischen Wörtern τόκος tókos „Geburt, Nachkommen“ und φέρειν phérein „tragen, bringen“ ab, da man einen Einfluss auf die Reproduktionsfähigkeit von Ratten als erstes entdeckte. Die Endsilbe „ol“ weist auf den chemischen Charakter eines Alkohols hin.
(RRR)-Tocopherole sind Bestandteile aller Membranen tierischer Zellen, werden jedoch nur von photosynthetisch aktiven Organismen wie Pflanzen und Cyanobakterien gebildet.
| Strukturformel | |
|---|---|
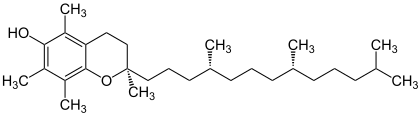
| |
| (RRR)-Isomer von Tocopherol (α-Tocopherol) | |
| Allgemeines | |
| Trivialname | Vitamin E |
| Andere Namen | |
| Summenformel | C29H50O2 |
| CAS-Nummer |
|
| PubChem | |
| ATC-Code | |
| DrugBank | |
| Kurzbeschreibung | gelbe bis braune Flüssigkeit |
| Vorkommen | Getreide, Nüsse, Samen, Pflanzenöle, Milch, Eier |
| Physiologie | |
| Funktion | Antioxidans |
| Täglicher Bedarf | 10 mg |
| Folgen bei Mangel | Unfruchtbarkeit, unspezifische Symptome wie: trockene, faltige Haut, Müdigkeit, verminderte Wundheilung |
| Überdosis | > 300 mg/Tag |
| Eigenschaften | |
| Molare Masse | 430,71 g/mol |
| Aggregatzustand | flüssig |
| Dichte | 0,95 g/cm3 |
| Schmelzpunkt | 2,5–3,5 °C |
| Siedepunkt |
|
| Löslichkeit | fettlöslich, < 1 mg/l in Wasser |
Geschichte
Vitamin E wurde als „Fruchtbarkeits-Vitamin“ entdeckt und als „Fortpflanzungsvitamin“ sowie als „Antisterilitätsvitamin“ beschrieben. Herbert M. Evans und Katherine S. Bishop wiesen 1922 als erste auf einen bis dahin unbekannten fettlöslichen Faktor hin, der für die Reproduktion von Ratten notwendig war. In den Folgejahren wurde dieser Faktor in Form von α-Tocopherol vor allem aus Weizenkeimöl, Hafer und Mais isoliert, als Vitamin erkannt und aufgrund der bereits bekannten Vitamine A, B, C und D nun Vitamin „E“ genannt. Die antioxidative Wirkung wurde durch Harold S. Olcott und Oliver H. Emerson 1937 beschrieben. 1938 wurde die Struktur von Vitamin E (hier α-Tocopherol) von Erhard Fernholz aufgeklärt, zudem kam es im gleichen Jahr zur ersten chemischen Synthese durch Paul Karrer.
1968 wurde Vitamin E als essentieller Nährstoff durch das Food and Nutrition Board anerkannt.
Beschreibung
Die Grundstruktur aller Vitamin-E-Formen bildet ein an Position 6 hydroxylierter Chromanring, dessen Methylierung diese in eine α-, β-, γ- oder δ-Form unterteilt. Durch unterschiedlich gesättigte Seitenketten werden wieder vier Familien unterschieden, nämlich die
- Tocopherole mit einer gesättigten Seitenkette
- Tocomonoenole (T1) und marinen Tocopherole (MDT) mit einer einfach ungesättigten Seitenkette und die
- Tocotrienole> (T3) mit einer dreifach ungesättigten Seitenkette.
Weitere natürlich vorkommende Tocopherole sind 5,7-Dimethyltocol und 7-Methyltocol. Beide wurden 1956 aus Reiskeimöl isoliert. Die Synthese für 5,7-Dimethyltocol erfolgte bereits 1938 und für 7-Methyltocol 1958.
Die C2-Position am Chormanring sowie die C4'- und C8'-Positionen der Phythylseitenkette bei Tocopherol sind chiral, es sind damit acht Stereoisomere möglich. Tocopherole liegen natürlicherseits ausschließlich in einer (RRR)-Konfiguration vor. Die natürlich vorkommende (RRR)-Form von Vitamin E wurde auch als D-Form bezeichnet (D-α-Tocopherol). Die synthetisch hergestellte Form bildet ein Gemisch aus acht Stereoisomeren (all-rac), sie wurde ehemals DL-Form genannt (DL-α-Tocopherol). Im Handel sind ferner Ester als Acetate, Succinate oder Nicotinate beziehbar.
Tocopherole erscheinen gelblich-braun bzw. bernsteinfarben und sind in Wasser unlöslich. In organischen Lösungsmitteln wie Aceton, Dichlormethan und Ether ist die Löslichkeit erhöht. Zwar sind Tocopherole oxidationsempfindlich (außer in veresterter Form), gegenüber Säuren und Alkalien aber sehr stabil. Bei Raumtemperatur ist Tocopherol flüssig-viskos.
| Name | Struktur der (RRR)-Isomere | R1 | R2 |
|---|---|---|---|
| α-Tocopherol | -Tocopherols_Structural_Formulae_V.1.svg.png) |
CH3 | CH3 |
| β-Tocopherol | CH3 | H | |
| γ-Tocopherol | H | CH3 | |
| δ-Tocopherol | H | H |
| Name | Struktur der (R)-Isomere | R1 | R2 |
|---|---|---|---|
| α-Tocotrienol | -Tocotrienol_(R3=CH3)_V.1.svg.png) |
CH3 | CH3 |
| β-Tocotrienol | CH3 | H | |
| γ-Tocotrienol | H | CH3 | |
| δ-Tocotrienol | H | H |
| Name | Struktur der (RRR)-Isomere | R1 | R2 |
|---|---|---|---|
| α-Tocomonoenol | -Tocomonoenols_Structural_Formulae_V.1.svg.png) |
CH3 | CH3 |
| β-Tocomonoenol | CH3 | H | |
| γ-Tocomonoenol | H | CH3 | |
| δ-Tocomonoenol | H | H |
| Name | Struktur der (RRR)-Isomere | R1 | R2 |
|---|---|---|---|
| α-MDT | -Tocomonoenols_terminal_Structural_Formulae_V.1.svg.png) |
CH3 | CH3 |
| β-MDT | CH3 | H | |
| γ-MDT | H | CH3 | |
| δ-MDT | H | H |
Plastochromanol
Plastochromanole sind eine Gruppe von Molekülen die von Pflanzen gegen die Lipidperoxidation produziert werden und die mögliche prooxidative Aktivität von α-Tocopherol verhindern können. Bei γ-Tocotrienol handelt es sich um Plastochromanol-3. Plastochromanole kommen beispielsweise in Leinöl, Leindotteröl, Sacha Inchi und Arabidopsis vor.
Aufgabe/Funktion im Körper
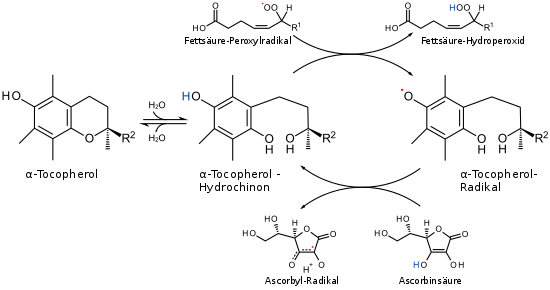
Eine seiner wichtigsten Funktionen ist die eines lipidlöslichen Antioxidans, das in der Lage ist, mehrfach ungesättigte Fettsäuren in Membranlipiden, Lipoproteinen und Depotfett vor einer Zerstörung durch Oxidation (Lipidperoxidation) zu schützen. Freie Radikale würden die Doppelbindungen der Fettsäuren der Zell- und Organellmembranen angreifen. Tocopherol wirkt als Radikalfänger, indem es selbst zu einem reaktionsträgen, da mesomeriestabilisierten Radikal wird. Das Tocopherol-Radikal wird dann unter Bildung eines Ascorbatradikals reduziert. Das Ascorbatradikal wird mit Hilfe von Glutathion (GSH) regeneriert. Dabei werden zwei Monomere (GSH) zu einem Dimer (GSSG) oxidiert.
Vitamin E hat Funktionen in der Steuerung der Keimdrüsen und wird daher auch als Antisterilitätsvitamin bezeichnet.
Der menschliche Körper kann am besten (RRR)-α-Tocopherol speichern und transportieren.
Im Blutplasma liegt insbesondere (RRR)-α-Tocopherol als Vitamin E-Form vor. Dies liegt daran, da das in der Leber gebildete α-Tocopherol-Transferprotein (α-TTP) bevorzugt diese Stereoisomer bindet. Es findet ferner eine Unterscheidung zwischen RRR- and SRR-α-Tocopherol-Stereoisomeren statt, da zur Bindung in einer Bindungstasche von α-TTP die R-stereochemische Konfiguration C2 vorliegen muss. Via α-TTP wird α-Tocopherol dann für den Transport im Blut in VLDL inkorporiert und schließlich in Form von HDL im Körper verteilt.
Durch die Speicherkapazität kann eine einmalige Gabe für längere Zeit wirken. Das im Wesentlichen in Sojaprodukten vorkommende γ-Tocopherol zeigt eine geringere Aktivität. Neuerdings wird aber diskutiert, ob diesem eine besondere Rolle zugeschrieben werden muss. In humanem LDL, einem Lipoprotein, sind α-Tocopherol und in geringer Konzentration auch γ-Tocopherol vorhanden.
Die biologische Aktivität unterscheidet sich unter den Vitameren. Bezogen auf α-Tocopherol (100 %) weist β-Tocopherol 50 %, γ-Tocopherol 10 %, δ-Tocopherol 3 %, α-Tocotrienol 30 % und β-Tocotrienol 5 % der Aktivität auf.
Besondere Eigenschaften von α-Tocopherol
α-Tocopherol, das am meisten verwendete und auch synthetisch hergestellte Isomer von Vitamin E hat einige positive und weniger positive Eigenschaften im Vergleich zu anderen Tocochromanolen:
- Es wird vom Transportprotein TTP in Säugetieren bevorzugt transportiert und in der Leber gespeichert.
- Es kann sogar pro-oxidativ wirken, also die Haltbarkeit von Lipiden (Speiseölen) verschlechtern. Diese pro-oxidative Wirkung wird von Plastochromanolen verhindert.
- Während sehr geringe Mengen die Cholesterinproduktion leicht drosseln, bewirken größere Mengen (im Tierversuch bei Meerschweinchen ab 5 mg/d) eine deutliche Steigerung des Plasma-Cholesterins.
- Die cholesterinsenkende Eigenschaft von Tocotrienolen wird durch alpha-Tocopherol stark reduziert.
Vorkommen
| Lebensmittel | Gehalt mg/100 g |
|---|---|
| Weizenkeimöl | 215,4 |
| Sonnenblumenöl | 55,8 |
| Erdnussöl | 17,2 |
| Olivenöl | 12,0 |
| Weizenkleie | 2,4 |
| Mais | 2,0 |
| Haferflocken | 1,5 |
| Spargel | 2,0 |
| Tomate | 0,9 |
| Möhre | 0,6 |
| Blumenkohl | 0,1 |
| Mandel | 25,0 |
| Haselnuss | 25,0 |
| Walnuss | 6,2 |
Tocopherol kommen sowohl in tierischen als auch pflanzlichen Nahrungsmitteln vor, wobei die Gehalte bei letzteren wesentlich höher sind. Besonders hohe Gehalte an Vitamin E weisen pflanzliche Öle auf, in der Regel überwiegt der Anteil von α-Tocopherol. Dagegen dominiert in Sojaöl γ-Tocopherol. Je mehr ungesättigte Fettsäuren in den Ölen enthalten ist, desto mehr Vitamin E kommt darin vor.
Gemüse enthält im Vergleich zu den Ölen wenig Vitamin E, allgemein kommt in grünen Pflanzenteilen abhängig von der Menge an Chloroplasten viel α-Tocopherol vor. Daneben findet man es auch in anderen, „gelben“ Pflanzenteilen wie Wurzeln oder Früchten, dort korreliert es mit dem Gehalt an Chromoplasten (überwiegend als γ-Tocopherol).
Vitamin E wird nur in Pflanzen aufgebaut, die Biosynthese startet aus Homogentisinsäure sowie Phytylpyrophosphat größtenteils in den Plastiden.
In Palmöl wurde auch α-Tocomonoenol nachgewiesen, während manche marinen Organismen das sogenannte marine Tocopherol (marine derived tocopherol, MDT) enthalten.
Bedarf
Der Mindestbedarf an Vitamin E beträgt 4 mg/d, zuzüglich etwa 0,4 mg pro Gramm Zufuhr an mehrfach ungesättigten Fettsäuren. Um die von verschiedenen Autoren als protektiv angesehenen Plasmaspiegel zu erreichen, ist eine Zufuhr von 20 bis 35 mg/d erforderlich. Aufgrund der geringen Toxizität werden teilweise Dosierungen von 268 mg/d empfohlen. Der Plasmaspiegel sollte oberhalb von 30 µmol/l liegen (bei einem Cholesterinwert von 220 mg/dl).
Mangelerscheinungen beim Menschen (Hypovitaminosen) sind heutzutage in Europa sehr selten, da Tocopherol sehr gut in der Leber und im Fettgewebe gespeichert werden kann. Nachgewiesene Mangelerscheinungen treten meist nur im Zusammenhang mit Krankheiten wie z. B. einer exokrinen Pankreasinsuffizienz oder einer Verminderung des Gallenflusses auf, bei denen gleichzeitig die Aufnahme von Fetten gestört ist.
Genauso wie die fettlöslichen Vitamine Vitamin A, Vitamin D und Vitamin K werden (RRR)-α-Tocopherol und die (2R)-Stereoisomere [(RSR)-, (RRS)- und (RSS)-α-Tocopherol] im Fettgewebe bzw. Blutplasma des Körpers angereichert. Die synthetisch hergestellten (2S)-Stereoisomere [(SRR)-, (SSR)-, (SRS)- und (SSS)-α-Tocopherol] werden hingegen nicht im Blutplasma gespeichert.
Das BfR hat auf Basis der sogenannten akzeptablen täglichen Aufnahmemenge (Acceptable Daily Intake, ADI) bei 0,15–2 mg/kg Körpergewicht neue Grenzen für eine akzeptable Tagesaufnahmemenge festgelegt. Bei einem Referenzkörpergewicht für Erwachsene von 70 kg entspricht diese 105–140 mg Vitamin E. Jugendliche der Altersgruppe der 15- bis 17-Jährigen haben ein Referenzgewicht von 61,3 kg, wodurch die tägliche Aufnahme von 92–123 mg Vitamin E als akzeptabel bewertet wird.
Das BfR schlägt für Nahrungsergänzungsmittel eine Höchstmenge von 30 mg pro Tag vor, warnt aber davor, dass bei Männern ab 55 Jahren bei einer unkontrollierten Supplementierung das Risiko für Prostatakrebs erhöht werden kann.
Pharmakoepidemiologische Untersuchungen zum Tocopherol
Zur Pharmakoepidemiologie des α-Tocopherols liegen umfangreiche Daten aus den Nationalen Untersuchungs-Surveys der Deutschen Herz-Kreislauf-Präventionsstudie (DHP) und aus dem Bundes-Gesundheitssurvey für die Bevölkerung vor. Durch die regelmäßige Anwendung α-tocopherolhaltiger Präparate kommt es danach zu einer dosisabhängigen und statistisch signifikanten Verringerung des β- und des γ-Tocopherols im Serum. Gesundheitliche Aspekte einer möglichen erhöhten Blutungsneigung unter Komedikation mit Acetylsalicylsäurepräparaten werden in der Literatur diskutiert. Auch zu Tocopheroloxidationsprodukten, wie z.B. dem Tocopherolchinon liegen Untersuchungsergebnisse aus Survey-Daten vor.
Auch aus der Berliner Studie an Vegetariern liegen Daten zum Gehalt an Tocopherolen im Serum der Studienteilnehmer vor. Trotz höherer Aufnahme an Tocopherolen waren die Tocopherolgehalte im Serum der Vegetarier niedriger als bei den Vergleichspersonen.
In einer großangelegten Studie an 35533 Männern wurde untersucht, ob Vitamin E gegen Prostatakrebs schützt. Verwendet wurden 400 IE/d all rac-α-tocopheryl acetate (synthetisch hergestelltes dl-α-Tocopherylacetat). Im Ergebnis trat Prostatakrebs zu 17 Prozent häufiger im Vergleich zur Kontrollgruppe auf. Dagegen wurde bei mehreren in vitro-Studien mit den gamma-Isomeren (gTP bzw. gTE) eine apoptotische Wirkung auf Prostatakrebszellen beobachtet. Zu ähnlich positiven Ergebnissen hinsichtlich der Schutzwirkung der Tocopherole kommt eine Multizentrische Studie mit mehr als 2000 Studienteilnehmern unter Berücksichtigung ernährungsepidemiologischer Daten zur Tocopherolaufnahme mit der Nahrung.
Verwendung
Tocopherole finden in der Lebensmittelindustrie als Antioxidationsmittel Verwendung. Sie sind in der EU als Lebensmittelzusatzstoffe der Nummern E 306 (Tocopherol-haltige Extrakte), E 307 (Alpha-), E 308 (Gamma-) und E 309 (Delta-Tocopherol) für alle für Zusatzstoffe zugelassenen Nahrungsmittel, zum Teil (in Form von tocopherolhaltigen Extrakten natürlichen Ursprungs) auch für „Bio“-Lebensmittel (E 306), zugelassen.
Neben Lebensmitteln wird Vitamin E auch Kosmetika (Sonnenschutzmitteln) und Anstrichmitteln zugesetzt sowie in künstlichen Gelenken zur höheren Beständigkeit gegen die Oxidation des verwendeten Kunststoffs. Bei Kondomen soll eine Vitamin-E-Beschichtung u.a. die Reißfestigkeit erhöhen.
Auch im Adjuvans AS03 im COVID-19-Impfstoff GBP510 findet DL-α-Tocopherol Verwendung.
Mit Sebacinsäure und Polyethylenglycol verestert erhält man das nichtionische Tensid Polyoxyethanyl-α-tocopherylsebacat (PTS), das als Hilfsmittel bei der Phasentransferkatalyse eingesetzt werden kann.
Analytik
Die heute fast ausschließlich eingesetzten Methoden zur zuverlässigen qualitativen und quantitativen Bestimmung der einzelnen Tocopherole sind die HPLC, die Gaschromatographie und die Kopplungsverfahren der HPLC-MS und der GC/MS mit der Probenvorbereitung der zu untersuchenden Öle durch die Anwendung der lipophilen Gelchromatographie an modifiziertem Sephadex LH 20. Beide Verfahren werden sowohl in der lebensmittelchemischen Analytik als auch bei pharmazeutischen und physiologischen Fragestellungen verwandt. Das Massenspektrum des Tocopherols findet sich auch in der Spektrenbibliothek des NIST. In Abhängigkeit von den zu untersuchenden Matrices empfehlen sich adäquate Probenvorbereitungsverfahren wie z.B. Extraktionsmethoden, auch unter Einsatz von Festphasenextraktionssäulen oder anderen Extraktionshilfsmitteln wie z.B. dem aus Diatomeenerde hergestellten Extrelut. Die früher häufig eingesetzten photometrischen Verfahren finden fast keine Verwendung mehr, da sie in der Regel keine Unterscheidung der einzelnen Tocopherole zulassen. Stereoisomere racemischen alpha-Tocopherols lassen sich sowohl durch HPLC als auch durch Gaschromatographie trennen.
Literatur
- Carlo Agostoni et al.: Scientific Opinion on Dietary Reference Values for vitamin E as α-tocopherol.
In: EFSA (Hrsg.): EFSA Journal. Band
13, Nr. 7, 2015,
doi:
 10.2903/j.efsa.2015.4149 (englisch).
10.2903/j.efsa.2015.4149 (englisch). - Klaus Pietrzik, Ines Golly, Dieter Loew: Handbuch Vitamine: Für Prophylaxe, Therapie und Beratung. 1. Auflage. Urban & Fischer, Elsevier, München 2008, ISBN 978-3-437-55361-5.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 11.02. 2026
