
1,3-Butadien
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK | Schweiz: 5 ml/m3 bzw. 11 mg/m3 | ||||||||
| Strukturformel | |
|---|---|
| Allgemeines | |
| Name | 1,3-Butadien |
| Andere Namen |
|
| Summenformel | C4H6 |
| Kurzbeschreibung | farbloses Gas mit aromatischem Geruch |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 106-99-0 |
| EG-Nummer | 203-450-8 |
| ECHA-InfoCard | 100.003.138 |
| PubChem | 7845 |
| Eigenschaften | |
| Molare Masse | 54,09 g/mol |
| Aggregatzustand | gasförmig |
| Dichte | 2,4982 kg/m3 (0 °C) |
| Schmelzpunkt | −108,92 °C |
| Siedepunkt | −4,5 °C |
| Dampfdruck | 239,8 kPa (20 °C) |
| Löslichkeit | wenig löslich in Wasser (1,03 g/l bei 20 °C) |
| Brechungsindex | 1,4292 (−25 °C) |
| Thermodynamische Eigenschaften | |
| ΔHf0 | 110,0 kJ/mol |
1,3-Butadien [-butaˈdi̯eːn] (Vinylethylen) ist ein farbloses Gas mit mildem, aromatischen Geruch. Es ist ein ungesättigter Kohlenwasserstoff von großer industrieller Bedeutung. Daneben existiert noch das schwieriger herzustellende und industriell weit weniger bedeutende 1,2-Butadien.
2-Methyl-1,3-butadien oder Isopren, die Grundeinheit der Terpene, ist ein Derivat des Butadiens.
Herstellung
Butadien wird technisch in erheblichen Mengen durch Wasserstoffabspaltung aus gesättigten Kohlenwasserstoffen durch starkes Erhitzen (Cracken) hergestellt. Im Labor wird der Zerfall von 3-Sulfolen in siedendem Xylol in einer [4+1]-Cycloeliminierung zu 1,3-Butadien und Schwefeldioxid verwendet.
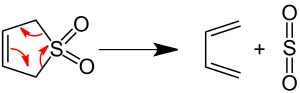
Eigenschaften
Die Geruchsschwelle von Butadien liegt bei 4 mg/m³. Das Gas lässt sich leicht verflüssigen. Butadien ist schwerer als Luft und in Wasser – mit 1,03 g/l bei 20 °C – nur sehr gering löslich.
Butadien ist brennbar und polymerisiert leicht, weswegen ihm meist ein Stabilisator wie das 4-tert-Butylbrenzcatechin (TBC) beigefügt wird. Die Polymerisationswärme beträgt −73 kJ·mol−1 bzw. −1350 kJ·kg−1.
Konjugierte Doppelbindungen beim 1,3-Butadien
| Konjugierte π-Bindung |
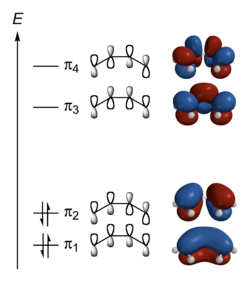 Delokalisiertes Molekülorbital bei 1,3-Butadien |
Im planar gebauten Molekül sind alle vier Kohlenstoffatome sp2-hybridisiert. Die π-Orbitale überlappen sich ober- und unterhalb der Molekülebene. π-Bindungen entstehen durch Überlappung bei dem 1. und 2. Kohlenstoffatom sowie dem 3. und 4. Kohlenstoffatom. Zusätzlich können aber die Orbitale des 2. und des 3. Kohlenstoffatoms überlappen, so dass sich die π-Elektronen über das ganze Molekül ausbreiten können. Die Elektronen sind delokalisiert. Dadurch, dass sich Elektronen auf einem größeren Raum verteilen, wird im 1,3-Butadien eine erhöhte Stabilität beobachtet. Der Einfluss dieser konjugierten Doppelbindungen zeigt sich bei Additionsreaktionen von Butadien: Es können sich 1,2- und 1,4-Addukte bilden. Im letzten Fall bildet sich zwischen dem 2. und dem 3. Atom eine „neue“ Doppelbindung. Analog verlaufen Polyadditionsreaktionen von Butadien, die zu 1,2-Polybutadien oder 1,4-Polybutadien führen. Das Verhältnis von 1,4- zu 1,2-Verknüpfung hängt stark von der Polymerisationsmethode und den Reaktionsbedingungen ab.
Verwendung
Mehr als 90 Prozent der Produktion von Butadien wird zu Synthesekautschuk weiterverarbeitet. Eine weitere Anwendung ist ABS, ein Terpolymerisat aus Acrylnitril, Butadien und Styrol. Außerdem wird aus Butadien und Blausäure in technischem Maßstab Adiponitril hergestellt, das ein Zwischenprodukt in der Produktion von Polyamiden ist. Aus Butadien werden Hydroxyl-terminierte Polybutadiene (HTPB) hergestellt, die als Treibstoff in Feststoffraketentriebwerken eingesetzt werden. Cyclobuten kann durch photochemische Cyclisierung von 1,3-Butadien erhalten werden:
![]()
Diese Methode verläuft allerdings nur mit 30%iger Ausbeute ab.
Historisches
Das aus Butadien und dem Katalysator Natrium produzierte Polymer Buna (ButadienNatrium) hatte große Bedeutung für die deutsche Rüstungs- und Kriegswirtschaft vor und während des Zweiten Weltkrieges.
Sicherheitshinweise
Butadien ist hochentzündlich. Zwischen einem Luftvolumenanteil von 1,4 bis 16,3 Prozent bildet es explosive Gemische. Butadien wirkt narkotisierend. Beim Menschen wirkt 1,3-Butadien krebserregend. Bei Industriearbeitern, die über längere Zeit einer Exposition mit 1,3-Butadien ausgesetzt waren, wurde eine erhöhte Anzahl an Krebserkrankungen festgestellt. Dabei handelte es sich vor allem um lympho-hämatopoetische Malignome (maligne Lymphome und Leukämien). Die Auswirkungen von 1,3-Butadien auf menschliche Gesundheit und Umwelt werden unter REACH im Jahr 2014 im Rahmen der Stoffbewertung von Deutschland geprüft.
Berufskrankheit
Seit August 2017 können bestimmte Erkrankungen durch 1,3-Butadien in Deutschland auf Antrag als Berufskrankheit anerkannt werden (Nummer 1320 der Anlage 1 zur Berufskrankheiten-Verordnung – BKV). Das gilt auch für solche Erkrankungen, die vor diesem Termin eingetreten sind (§ 6 Abs.1 BKV).


© biancahoegel.de;
Datum der letzten Änderung: Jena, den: 19.08. 2024


