
Eisen(III)-hydroxidoxid
| Sicherheitshinweise | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
Eisen(III)-hydroxidoxid ist eine anorganische chemische Verbindung mit der Zusammensetzung FeO(OH). Dies kann bei gleichem Verhältnis der Elemente auch als Fe2O3·H2O geschrieben werden; es gehört damit zur Gruppe der Eisenhydroxide oder Eisen(III)-oxidhydrate, die sich im Grad ihrer Hydratation unterscheiden.
Vorkommen
| Kristallstruktur | |
|---|---|
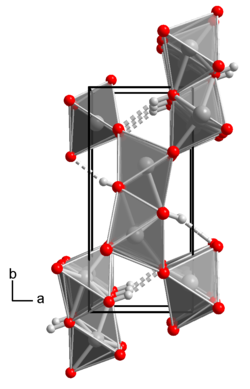
| |
| _
Fe2+
_
O2−
_
H+
Wasserstoffbrückenbindungen sind als gestrichelte Linien gezeichnet | |
| Allgemeines | |
| Name | Eisen(III)-hydroxidoxid |
| Andere Namen |
|
| Verhältnisformel | FeO(OH) |
| Kurzbeschreibung | gelbes geruchloses Pulver |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer |
|
| ECHA-InfoCard | 100.039.754 |
| PubChem | 91502 |
| DrugBank | DB14695 |
| Eigenschaften | |
| Molare Masse | 88,86 g/mol |
| Aggregatzustand | fest |
| Dichte | 4,1 g/cm3 |
| Schmelzpunkt | > 180 °C (Zersetzung) |
| Löslichkeit | praktisch unlöslich in Wasser |
α–Eisen(III)-hydroxidoxid kommt in der Natur als Mineral Goethit (auch Nadeleisenerz) vor, die β–Form als Akaganeit, die γ–Form als Lepidokrokit (Rubinglimmer) und die δ–Form als Feroxyhyt.
Gewinnung und Darstellung
-hydroxid.jpg)
α-Eisen(III)-hydroxidoxid ist ein rostfarbener, voluminöser Niederschlag, der aus Eisen(III)-Salzlösungen (z. B. Eisen(III)-nitrat) beim Versetzen mit Hydroxidionen ausfällt.
γ-Eisen(III)-hydroxidoxid erhält man durch Reaktion von Eisen(II)-chlorid-Tetrahydrat mit Hexamethylentetramin und Reaktion des Zwischenproduktes Eisen(II)-hydroxid mit einer Natriumnitritlösung.
Industriell wird zur Herstellung gelben Eisen (III)-hydroxidoxids häufig der Laux-Prozess angewandt, bei dem Späne aus Gusseisen in Anwesenheit von Wasser mit Nitrobenzol oxidiert und Letzteres gleichzeitig zu Anilin reduziert wird.
Eigenschaften

Der Niederschlag löst sich leicht in Säuren, ist im basischen Milieu jedoch praktisch unlöslich. Dieses nützt man z.B. beim Kationentrennungsgang zur Abtrennung von Eisen aus.
Nur mit heißen konzentrierten Basen kann man Hydroxoferrate(III) herstellen. Beim Erwärmen geht Eisen(III)-oxidhydroxid in α-Fe2O3 über.
α-Eisen(III)-hydroxidoxid hat eine orthorhombische Kristallstruktur, isotyp zu der von Diaspor (Raumgruppe Pbnm (Raumgruppen-Nr. 62, Stellung 3); a = 464 pm, b = 1000 pm, c = 303 pm).
γ-Eisen(III)-hydroxidoxid ist ein aus äußerst feinen Nädelchen bestehendes, leicht stäubendes Pulver von tieforangeroter Farbe. Es kann durch Erhitzen im Vakuum oder trockenen Luftstrom im Bereich von etwa 250 bis 400 °C in reines y-Fe2O3 übergeführt werden. Bei höherem Erhitzen oder schon bei sehr intensivem Zerreiben entsteht aus den metastabilen Präparaten der γ-Reihe über metastabiles β-FeO(OH) die stabile α-Modifikation. Die γ-Modifikation besitzt eine orthorhombische Kristallstruktur (Raumgruppe Bbmm (Nr. 63, Stellung 5), a = 1240 pm, b = 387 pm, c = 306 pm).
Verwendung
Eisen(III)-hydroxide dienen seit altersher unter der Bezeichnung "Ocker" als Pigmente für gelbe, rote und braune Farbtöne. Sie sind lichtecht, können ihre Farbe aber bei Erhitzen (Abspaltung von Wasser) ändern (Rotfärbung). Eisen(III)-hydroxidoxid wird in granulierter Form als Adsorptionsmittel in der Wasseraufbereitung eingesetzt. Die weltweit wichtigste Anwendung ist hierbei die Entfernung von Arsen aus Trinkwasser mit Hilfe von Adsorptionsfiltern. Eisen(III)-hydroxidoxid ist in Deutschland entsprechend der §11-Liste des Umweltbundesamtes (UBA) als Aufbereitungsstoff für Trinkwasser zugelassen. Voraussetzung ist, dass das Granulat den Qualitätsanforderungen der Europäischen Norm EN DIN 15029 entspricht. Ein anderes Anwendungsgebiet ist die Entfernung von Phosphat aus Oberflächenwasser. So wird Eisen(III)-hydroxidoxid in Adsorptionsfiltern zur Nährstoffelimination verwendet und bekämpft die Gefahr der Eutrophierung von Seen. Auch im Aquaristik-Bereich wird Eisen(III)-hydroxidoxid zu diesem Zweck eingesetzt und verhindert übermäßiges Algenwachstum.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 19.12. 2023