Iodmethan
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK |
| ||||||||
| Toxikologische Daten | 76 mg/kg (LD50, Ratte, oral) | ||||||||
Iodmethan, veraltet Methyliodid, ist eine organische Halogenverbindung.
| Strukturformel | ||
|---|---|---|
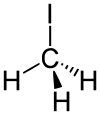 | ||
| Allgemeines | ||
| Name | Iodmethan | |
| Andere Namen |
| |
| Summenformel | CH3I | |
| Kurzbeschreibung | farblose, stechend etherisch riechende Flüssigkeit | |
| Externe Identifikatoren/Datenbanken | ||
| EG-Nummer | 200-819-5 | |
| ECHA-InfoCard | 100.000.745 | |
| PubChem | 6328 | |
| Eigenschaften | ||
| Molare Masse | 141,94 g/mol | |
| Aggregatzustand | flüssig | |
| Dichte | 2,28 g/cm3 | |
| Schmelzpunkt | −66 °C | |
| Siedepunkt | 42 °C | |
| Dampfdruck |
| |
| Löslichkeit | schlecht in Wasser (8,66 g/l bei 20 °C) | |
| Dipolmoment | 1,62 D (5,4 · 10−30 C · m) | |
| Brechungsindex | 1,5304 | |
| Thermodynamische Eigenschaften | ||
| ΔHf0 | −13,6 ± 0,5 kJ·mol−1 | |
Darstellung
Iodmethan entsteht in einer exothermen Reaktion, wenn Iod zu einem Gemisch von Methanol und rotem Phosphor gegeben wird. Das iodierende Reagenz ist Phosphortriiodid, das in situ gebildet wird:
Alternativ kann Iodmethan durch Reaktion von Dimethylsulfat mit Kaliumiodid in Gegenwart von Calciumcarbonat hergestellt werden:
Methyliodid/CH3I kann durch Destillation und nachfolgendes Waschen mit Na2S2O3 von Iod gereinigt werden.
Physikalische Eigenschaften
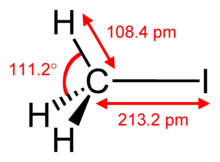
Iodmethan ist bei Umgebungstemperatur und Normaldruck eine farblose, etherisch riechende Flüssigkeit. Bei Normaldruck siedet die Verbindung bei 42,44 °C. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,1554, B = 1177,78 und C = −32,058 im Temperaturbereich von 218 bis 315,6 K bzw. mit A = 4,14897, B = 1223,831 und C = −20.179 im Temperaturbereich von 315,6 bis 521 K. Die Verbindung ist schwer brennbar. Der Explosionsbereich liegt zwischen 8,5 Vol.‑% (500 g/m3) als untere Explosionsgrenze (UEG) und 66 Vol.‑% (3870 g/m3) als obere Explosionsgrenze (OEG). Die Zündtemperatur beträgt 355 °C. Der Stoff fällt somit in die Temperaturklasse T2.
Chemische Eigenschaften
Iodmethan reagiert mit Alkali- und Erdalkalimetallen und wird zur Methylierung (Einführung einer Methylgruppe) von organischen Substanzen verwendet. Ammoniak und Amine reagieren mit Iodmethan unter Bildung von Methylammoniumiodiden. Durch Wiederholung dieser Reaktion können quartäre Ammoniumionen erzeugt werden (sog. erschöpfende Methylierung), wobei nach jedem Schritt das Amin mit einer Base freigesetzt wird:
Quartäre Ammoniumionen können nicht mehr durch Laugen deprotoniert werden. Ihre Salze sind vollständig dissoziiert.
Toxische Eigenschaften
Iodmethan hat sich im Tierversuch als krebserregend erwiesen.
Physiologische Wirkung
Iodmethan ist wie andere Methylierungsreagenzien (Beispiel: Dimethylsulfat) krebserregend und sehr toxisch. Die karzinogene Wirkung ist ursächlich verbunden mit der methylierenden Wirkung. Methyliodid ist ein sehr gutes Elektrophil und geht somit leicht nucleophile Substitutionsreaktionen mit körpereigenen Nucleophilen ein. Dadurch kommt es zu einer Methylierung der DNA, die dann bei der Zellteilung nicht mehr korrekt von der DNA-Polymerase abgelesen werden kann.
Reaktionen
Monsanto-Prozess
Iodmethan ist Bestandteil des katalytischen Zyklus des Monsanto-Prozess zu Herstellung von Essigsäure.
Verwendung
Durch Reaktion mit Natriumarsenit in Gegenwart von Natriumhydroxid kann Dinatriummethylarsonat gewonnen werden.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 08.03. 2025