
Iodpentafluorid
| Sicherheitshinweise | |||
|---|---|---|---|
|
Iodpentafluorid ist eine Interhalogenverbindung, die aus den Elementen Iod und Fluor im Verhältnis 1:5 besteht.
Gewinnung und Darstellung
Iodpentafluorid kann aus den Elementen hergestellt werden, indem man Iod in Fluor verbrennt.
| Strukturformel | |
|---|---|
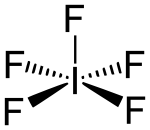 | |
| Allgemeines | |
| Name | Iodpentafluorid |
| Summenformel | IF5 |
| Kurzbeschreibung | farblose, an der Luft rauchende, stechend riechende Flüssigkeit |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 7783-66-6 |
| EG-Nummer | 232-019-7 |
| ECHA-InfoCard | 100.029.108 |
| PubChem | 522683 |
| Eigenschaften | |
| Molare Masse | 221,9 g/mol |
| Aggregatzustand | flüssig |
| Dichte | 3,21 g/cm3 |
| Schmelzpunkt | 9,4 °C |
| Siedepunkt | 100,5 °C |
Eigenschaften
Iodpentafluorid ist eine hochreaktive, stechend riechende, farblose und an
der Luft rauchende Flüssigkeit, die die Atmungsorgane heftig angreift
und mit wasserstoffreichen organischen Verbindungen unter Flammenerscheinung und
Bildung von Fluorwasserstoffsäure
reagiert. Mit Lewis-Säuren
und -Basen bildet sie die korrespondierenden Salze. Sie besitzt eine
Verdampfungswärme von 41,37 kJ/mol und eine Schmelzwärme von
15,91 kJ/mol.
Die elektrische
Leitfähigkeit beträgt 1,53·10−3S/m.
Iodpentafluorid ist hydrolyseempfindlich und reagiert mit Wasser heftig zu Iodsäure und Fluorwasserstoff:
Molekülgeometrie
Gasförmiges Iodpentafluorid besitzt gemäß dem VSEPR-Modell eine quadratisch-pyramidale Molekülgeometrie. Die vier FIF-Winkel betragen dabei 81,9°. Die axiale I–F-Bindung, welche die Spitze der quadratischen Pyramide bildet, besitzt eine Länge von 184,4 pm. Die vier planaren I–F-Bindungen, welche die quadratische Grundfläche der Pyramide bilden, haben eine Länge von 186,9 pm. Das freie Elektronenpaar am Iod-Atom ist dabei axial angeordnet, um einen möglichst großen Abstand zu den Fluor-Atomen zu gewährleisten.
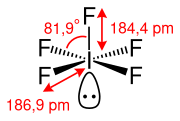
Iodpentafluorid besitzt als Molekülsymmetrie die Punktgruppe C4v.
Verwendung
Iodpentafluorid wird als fluorierendes Reagens in der organischen Chemie und als Ätzmittel in der Halbleiterindustrie eingesetzt.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 05.05. 2024