
Tetrafluormethan
| Sicherheitshinweise | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| Treibhauspotential | 7349 (bezogen auf 100 Jahre) | ||||||
Tetrafluormethan (auch Tetrafluorkohlenstoff) ist eine chemische Verbindung aus der Reihe der Fluorkohlenwasserstoffe. Bei ihm sind alle Wasserstoffatome des Methans durch Fluoratome substituiert. Beide Bezeichnungen sind nach der IUPAC-Nomenklatur korrekt, abhängig davon, ob die Verbindung als organische (Tetrafluormethan) oder anorganische (Tetrafluorkohlenstoff) Verbindung angesehen wird.
| Strukturformel | ||
|---|---|---|
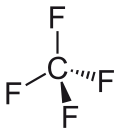 | ||
| Keile zur Verdeutlichung der Geometrie | ||
| Allgemeines | ||
| Name | Tetrafluormethan | |
| Andere Namen |
| |
| Summenformel | CF4 | |
| Kurzbeschreibung | geruch- und farbloses Gas | |
| Externe Identifikatoren/Datenbanken | ||
| CAS-Nummer | 75-73-0 | |
| EG-Nummer | 200-896-5 | |
| ECHA-InfoCard | 100.000.815 | |
| PubChem | 6393 | |
| Eigenschaften | ||
| Molare Masse | 88,01 g/mol | |
| Aggregatzustand | gasförmig | |
| Dichte | 3,72 kg/m3 (15 °C, 1013 mbar) | |
| Schmelzpunkt | −184 °C | |
| Siedepunkt | −128 °C | |
| Löslichkeit | schwer in Wasser (20 mg/l bei 20 °C) | |
| Thermodynamische Eigenschaften | ||
| ΔHf0 | −933,6 kJ/mol | |
Darstellung
Tetrafluormethan kann einerseits durch Verbrennung von Kohlenstoff in Fluor, andererseits durch elektrische Entladung in einem Kohlenstoffmonoxid-Fluorgemisch dargestellt werden:
Eine weitere Methode ist die Umsetzung von Siliciumcarbid mit Fluor zu Tetrafluormethan und Siliciumtetrafluorid:
Die Umsetzung ist nahezu quantitativ, und die gasförmige Siliciumverbindung kann aus dem Gasgemisch durch Waschen mit einer Natriumhydroxidlösung (Hydrolyse) entfernt werden.
Eigenschaften
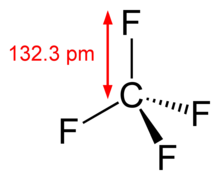
Physikalische Eigenschaften
Tetrafluormethan ist ein farb- und geruchloses Gas mit einem Schmelzpunkt von −184 °C und einem Siedepunkt von −128 °C. Tetrafluormethan ist in Wasser sehr schlecht (20 mg pro kg Wasser bei 20 °C) löslich, in Ethanol (ca. 80 mg pro kg Ethanol bei 25 °C) und Benzol (ca. 64 mg pro kg Benzol bei 25 °C) etwas besser.
Chemische Eigenschaften
Tetrafluormethan ist sehr reaktionsträge und wird von Säuren und Laugen nicht angegriffen. Lediglich siedende Alkalimetalle und heiße Alkalimetalldämpfe vermögen es langsam anzugreifen. Durch thermische Zersetzung oberhalb 1000 °C entstehen giftige Stoffe (Carbonylfluorid, Kohlenstoffmonoxid), in Gegenwart von Wasser auch der aggressive Fluorwasserstoff.
Es besitzt ein Treibhauspotential von 7349 und ist damit ein extrem starkes Treibhausgas.
Verwendung und Emissionen
Tetrafluormethan wird als Kältemittel zum Ersatz von FCKWs verwendet, da es keine abbauende Wirkung auf die Ozonschicht hat. Aufgrund des hohen Treibhauspotenzials jedoch wird in der F-Gase-Verordnung festgelegt, dass Anlagen mit den entsprechenden Gasen möglichst geringe Leckmengen abgeben sollen. Große Mengen Tetrafluormethan werden bei der Aluminiumerzeugung freigesetzt.
Toxikologie
Tetrafluormethan gilt als ungiftig. Es kann jedoch in geschlossenen Räumen durch Verdrängen der Luft zur Erstickung führen. Bei geringeren Konzentrationen ist eine narkotische Wirkung möglich.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 04.11. 2023
