
Ethylbenzol
| Sicherheitshinweise | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| MAK |
| ||||||||
| Toxikologische Daten |
| ||||||||
Ethylbenzol (Ethylbenzen, Phenylethan) ist eine farblose, benzolähnlich riechende Flüssigkeit. Es ist ein aromatischer Kohlenwasserstoff mit der Summenformel C8H10.
| Strukturformel | |
|---|---|
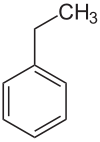 | |
| Allgemeines | |
| Name | Ethylbenzol |
| Andere Namen |
|
| Summenformel | C8H10 |
| Kurzbeschreibung | farblose Flüssigkeit |
| Externe Identifikatoren/Datenbanken | |
| CAS-Nummer | 100-41-4 |
| EG-Nummer | 202-849-4 |
| ECHA-InfoCard | 100.002.591 |
| PubChem | 7500 |
| Eigenschaften | |
| Molare Masse | 106,17 g/mol |
| Aggregatzustand | flüssig |
| Dichte | 0,87 g/cm3 |
| Schmelzpunkt | −95 °C |
| Siedepunkt | 136 °C |
| Dampfdruck |
|
| Löslichkeit | schwer in Wasser (170 mg/l bei 25 °C) |
| Brechungsindex | 1,49594 (20 °C) |
Darstellung
Ethylbenzol wird in der Industrie an einem Katalysator durch Alkylierung von Benzol mit Ethen hergestellt, hierbei gibt es die Flüssigphasen-Alkylierung und die Gasphasen-Alkylierung. Sehr wenig Ethylbenzol wird über Feinfraktionierung aus der C8-Aromatenfraktion isoliert. Dieses Verfahren wird auch Superfraktion genannt, ist jedoch gegenüber der Alkylierung nicht konkurrenzfähig.
Im Labor kann Ethylbenzol durch Wolff-Kishner-Reaktion aus Acetophenon hergestellt werden.
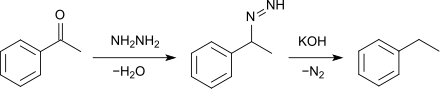
Eigenschaften
Ethylbenzol ist eine farblose, benzolähnlich riechende Flüssigkeit mit einem Schmelzpunkt von −95 °C und einem Siedepunkt von 136 °C. Bei dieser Temperatur beträgt die molare Verdampfungsenthalpie 35,57 kJ/mol.
-
Parameter für die Antoine-Gleichung
(nach lg P = A−B/(T+C) )A B C T 4,07488 1419,315 −60,539 329,74–410,27 K 4,40536 1695,026 −23,698 420–600 K
In Wasser ist es unlöslich, in organischen Lösungsmitteln jedoch löslich.
Metabolismus
Im Körper wird der Ethylrest des Ethylbenzols oxidiert. Zwischenprodukte im Metabolismus sind Phenylessigsäure und 1-Phenylethanol (Methylphenylcarbinol), das Endprodukt ist Mandelsäure, die genügend wasserlöslich ist, um über den Harn ausgeschieden zu werden.
Sicherheitstechnische Kenngrößen
Ethylbenzol gilt als entzündliche Flüssigkeit. Oberhalb des Flammpunktes können sich entzündliche Dampf-Luft-Gemische bilden. Die Verbindung hat einen Flammpunkt bei 23 °C. Der Explosionsbereich liegt zwischen 1 Vol.‑% (43 g/m3) als untere Explosionsgrenze (UEG) und 7,8 Vol.‑% (340 g/m3) als obere Explosionsgrenze (OEG). Die Zündtemperatur beträgt 430 °C. Der Stoff fällt somit in die Temperaturklasse T2. Er wird als gesundheitsschädlich eingestuft.
Verwendung
Ethylbenzol wird Benzin zur Erhöhung der Oktanzahl (Klopffestigkeit) beigemengt. Es ist Lösungsmittel für Farben und findet sich in Kunststoffen. Es ist wichtiger Ausgangsstoff für die Synthese des Styrols. Neben dem Benzol und dem Toluol gehört Ethylbenzol zu den technisch wichtigen Aromaten, den so genannten BTEX-Aromaten.
Literatur
- Ethylbenzol (hrsg. vom Beratergremium für Umweltrelevante Altstoffe (BUA) der Gesellschaft Deutscher Chemiker), S. Hirzel Verlag GmbH & Co, 1996, ISBN 3-7776-0722-3.
- Jochen Ackermann: Reaktionstechnische Untersuchungen zur Synthese von Ethylbenzol aus 1,3-Butadien unter Verwendung basischer Feststoffkatalysatoren. Shaker Verlag GmbH (2001), ISBN 3-8265-9254-9.
- Albrecht Xahil Tribukait: Untersuchung zum Einfluß des Drehimpulses auf die Dissoziationsgeschwindigkeit von Toluol und Ethylbenzol. Cuvillier (1999), ISBN 3-89712-536-6.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 13.12. 2024


