Massenbilanz (Thermodynamik)

Die Massenbilanz ist eine Bilanzgleichung der Thermodynamik und betrachtet die über die Systemgrenze ein- und austretenden Massenströme.
Allgemeine Gleichung der Massenbilanz
In einem geschlossenen System ist die Betrachtung der Masse trivial: Da keine Masse über die Systemgrenze gelangen kann, bleibt die Masse im System stets konstant. In einem offenen System hingegen kann Masse mit der Umgebung ausgetauscht werden. Diese Massenströme mit der Umgebung werden von der Massenbilanz erfasst. Für die Massenbilanz eines Reinstoffs gilt
Dabei ist :
die Gesamtmasse innerhalb der Systemgrenze
der über die Systemgrenze eintretende Massenstrom
der über die Systemgrenze austretende Massenstrom
die Zeit.
Gibt es mehrere ein- oder austretende Massenströme, wird die Massenbilanz verallgemeinert und die Summe der Massenströme betrachtet.
Durch die in der Regel verwendete Vorzeichenkonvention werden eintretende Massenströme positiv, austretende Massenströme negativ gezählt.
Im Rahmen der Relativitätstheorie ist es möglich, dass Masse innerhalb eines Systems zu Energie umgewandelt wird. Die Massenbilanz der Thermodynamik betrachtet derartige Effekte nicht.
Massenbilanz für einen stationären Prozess
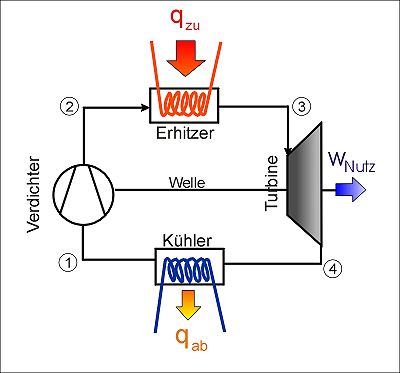
Liegt ein stationärer Prozess, beispielsweise ein Kreisprozess vor, ist die Änderung der Gesamtmasse gleich Null. Die Massenströme sind nicht mehr zeitabhängig, es gilt
oder für mehrere Massenströme
.
Massenbilanz bei Gemischen
Bei einem Gemisch gilt, sofern keine Reaktion stattfindet, die Erhaltung der Massen der einzelnen Komponenten. Soll die Gesamtmasse dieses Gemischs bilanziert werden, stellt man für jede Komponente eine eigene Massenbilanz auf.
Massenbilanz bei Reaktionen
Findet eine chemische Reaktion statt, so gilt die Erhaltung der Massen der einzelnen Komponenten nicht mehr. Die Masse der Edukte ist jedoch gleich der Masse der Produkte. Die Massenbilanz bilanziert nun keine Massenströme, sondern die Gesamtmassen der Komponenten. Für die Massenbilanz werden die stöchiometrischen Koeffizienten mit den Molmassen der einzelnen Stoffe multipliziert. So gilt für die Reaktion
die Massenbilanz
Man erhält diese Massenbilanz durch
Dabei ist
der jeweilige stöchiometrische Koeffizient
die Masse des jeweiligen Stoffes
die Molmasse des jeweiligen Stoffes.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 29.07. 2020