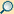Virusklassifikation
Die Klassifikation von Viren beruht auf verschiedenen morphologischen, epidemiologischen oder biologischen Merkmalen. Von der rein funktionellen Klassifikation ist jedoch die offiziell gültige Taxonomie von Viren zu unterscheiden, nach der Viren beispielsweise in Familien, Gattungen und Arten nach dem Grad ihrer Verwandtschaft (ermittelt insbesondere durch Genomvergleich) eingeteilt werden. Alle anderen Klassifikationen sind noch zum Teil aus historischen oder praktischen Gründen üblich. Die Entscheidung über Kriterien der Taxonomie und Einteilung von Viren trifft ein internationales Gremium mit dem Namen International Committee on Taxonomy of Viruses (ICTV).
Das klassische System der Virusklassifikation
Im Jahre 1962 wurde von André Lwoff, Robert W. Horne und Paul Tournier entsprechend der von Carl von Linné begründeten binären Klassifikation der Lebewesen eine Taxonomie der Viren („LHT-System“) eingeführt. In ihr werden analog zur Taxonomie anderer Lebewesen, die folgenden Taxa unterteilt:
- Virosphäre (Phylum: Vira)
Eine historische Einteilung der Viren nach dem LHT-System findet sich bei Francesco Fiume.[1] Die entscheidenden Charakteristika für diese Klassifikation waren:
- die Natur des viralen Genoms (DNA oder RNA)
- die Symmetrie des Kapsids
- Vorhandensein einer Lipidumhüllung
- Größe von Virion und Kapsid
Die drei morphologischen Kriterien (2–4) bestimmen den Morphotyp (Morphovar).
Frühe Klassifizierungssysteme berücksichtigten anstelle der noch nicht allgemein verfügbaren Genomsequenz folgende Kriterien:
- gemeinsame Organismen, die sie infizieren (Wirte)
- gemeinsame Übertragungswege, z. B. Vektoren
- ähnliche Krankheitsbilder (Symptome) bzw. Infektion des gleichen Organs
- Serotyp (Serovar)
- Habitat (Vorkommen)
- Klassifikation nach Wirten
- Bakterienviren (Bakteriophagen) – infizieren Bakterien
- Cyanophagen – infizieren Cyanobakterien (alias Blaugrünbakterien, veraltet: „Blaualgen“)
- Aktinobakteriophagen — infizieren Bakterien der Klasse Actinobacteria (Aktinobakterien)
- Corynephagen — infizieren Aktinobakterien der Gattung Corynebacterium (Corynebakterien)
- Mykobakteriophagen — infizieren Aktinobakterien der Gattung Mycobacterium (Mykobakterien)
- Vibriophagen — infizieren Bakterien der Gattung Vibrio (Vibrionen)
- Coliphagen — infizieren Escherichia coli (Colibakterien)
- Archaeenviren (der veralteten Bezeichnung „Archaebakterien“ folgend traditionell auch Bakteriophagen genannt) – infizieren Archaeen
- Magroviren – infizieren Archaeen der Marine Group II (d. h. der Ordnung Poseidoniales, Euryarchaeota)
- Asgardviren – infizieren Asgard-Archaeen
- Viren der Eukaryoten:
- Mykoviren – infizieren Pilze
- Phytoviren – infizieren Pflanzen
- Tierviren – infizieren Tiere (inkl. Menschen als Primaten)
- Insektenviren
- Bienenviren
- humanpathogene Viren – infizieren den Menschen
- Virophagen − benötigen ein Helfervirus und schädigen dieses
- Klassifikation nach Krankheitsbildern
- Onkoviren – karzinogen
- Hepatitis-Viren
- Influenzaviren (früheres Taxon) — verursachen Influenza (echte Grippe)
- Rhinoviren — verursachen grippale Infekte
- Nekroseviren
- Mosaikvirus
- Klassifikation nach Übertragungsweg
- Arboviren – Arthropoden (Gliederfüßer) als Vektoren
- Klassifikation nach Morphotyp (Morphologie des Virions) oder einfach nach Größe (von Kapsid oder Genom):
- Podoviren
- Myoviren
- Siphoviren
- Riesenviren
- Jumbophagen, Megaphagen
- Klassifikation nach Habitat (Vorkommen)
- Haloviren – salzliebend bzw. salzliebende Organismen parasitierend
- Bodenviren – infizieren Mikroben (insbesondere Archaeen) des Erdbodens
- Marine Viren
- Süßwasserviren
- Bodenviren
- Kombination der beschriebenen Kriterien
- Cyanopodovirus – Morphotyp: Podoviren, Wirte: Cyanobakterien
- Cyanomyovirus – Morphotyp: Myoviren, Wirte: Cyanobakterien
- Cyanostylvirus – Morphotyp: Siphoviren, Wirte: Cyanobakterien
- andere Kriterien
- Helfervirus – wird von einem Satellitenvirus zu dessen Replikation genutzt
- Satellitenvirus – kann sich ohne die Hilfe eines anderen Virus (Helfervirus) nicht im Wirt replizieren (siehe Symbiose). Es kann dessen Replikation erkennbar beeinträchtigen (Virophage), muss aber nicht.
In der modernen Taxonomie bleiben diese Kriterien unberücksichtigt, auch wenn sie weiter für die Zusammenfassung unterschiedlicher Viren mit gemeinsamen medizinischen oder epidemiologischen Merkmalen wichtig sind.
Virustaxonomie nach ICTV
Die moderne Virus-Taxonomie nach ICTV orientiert sich ebenfalls nach Linné. Sie umfasst seit 2018 auch die höheren Rangstufen oberhalb der Ordnung, mit Namensendungen, die teilweise vom LHT-System abweichen.[2][3]
- Realm (en. realm) (…viria)
- Subrealm (en. subrealm) (…vira) (Endung wie bei Subphylum im LHC-System, als zweiteoberste Stufe)
- Reich (en. kingdom) (…virae)
- Unterreich (en. subkingdom) (…virites)
- Stamm oder Phylum (…viricota) (in Analogie zu …archaeota - abweichend vom LHC-System sind mehrere Virusphyla möglich)
- Subphylum (…viricotina)
- Klasse (…viricetes)
- Unterklasse (…viricetidae)
- Ordnung (…virales)
- Unterordnung (…virineae)
- Familie (…viridae)
- Unterfamilie (…virinae)
- Gattung oder Genus (…virus)
- Untergattung oder Subgenus (…virus)
- Art oder Species (…virus)
- Untergattung oder Subgenus (…virus)
- Gattung oder Genus (…virus)
- Unterfamilie (…virinae)
- Familie (…viridae)
- Unterordnung (…virineae)
- Ordnung (…virales)
- Unterklasse (…viricetidae)
- Klasse (…viricetes)
- Subphylum (…viricotina)
- Stamm oder Phylum (…viricota) (in Analogie zu …archaeota - abweichend vom LHC-System sind mehrere Virusphyla möglich)
- Unterreich (en. subkingdom) (…virites)
- Reich (en. kingdom) (…virae)
- Subrealm (en. subrealm) (…vira) (Endung wie bei Subphylum im LHC-System, als zweiteoberste Stufe)
Mit Ende Juni 2022 gibt es sechs vom ICTV anerkannte Realms, die sich wie folgt unterteilen:[4]
- Realm Adnaviria (Baltimore 1)
- Realm Duplodnaviria (Baltimore 1)
- Realm Monodnaviria (Baltimore 1 und 2)
- Realm Riboviria (Baltimore 3 bis 7)
- Realm Ribozyviria (Gattung Deltavirus und ähnliche; ~ Baltimore 5, aber Satellitenviren mit zirkulärer RNA)
- Realm Varidnaviria (Baltimore 1)
- nicht-zugeordnete Taxa:
- 1 Klasse: Naldaviricetes (Baltimore 1)
- 22 Familien
- 2 Gattungen
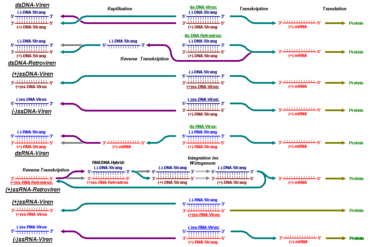
Die Baltimore-Klassifikation
Auf Grundlage des Wissens um die Molekularbiologie der Viren hatte sich seit 1971 eine weitere Klassifikation etabliert, welche auf einen Vorschlag des Nobelpreisträgers David Baltimore zurückgeht.[5][6]
Wichtige Kriterien dieser Klassifizierung sind:
- Genomstruktur
- Form (Symmetrie) des Kapsids
- Vorhandensein einer Hülle
- Anordnung der Gene innerhalb des Genoms
- Replikationsstrategie
- Virusgröße
Die verschiedenen Möglichkeiten ergeben sich dadurch, dass ein Strang der doppelsträngigen DNA, so wie sie in allen zellulären Organismen vorliegt, redundant ist und bei Viren daher entfallen kann. Ebenso kann das Virusgenom auch in verschiedenen Formen der RNA vorliegen, die in Zellen als Zwischenstufe bei der Proteinsynthese (mRNA) auftritt. Bei einzelsträngiger DNA oder RNA kommen beide möglichen Kodierungsrichtungen vor: die normale Richtung 5'→3', die als (+) Polarität bezeichnet wird, wie sie in der mRNA vorliegt, und die entgegengesetzte (komplementäre) Richtung (-), in der die RNA quasi als Negativ vorliegt.[7]
Diese Baltimore-Klassifikation nach der Replikationsstrategie wird heute zunehmend ungebräuchlich, denn
- seit 2018 stehen durch das ICTV definierte hohe Rangstufen (oderhalb der Ordnung) zur Verfügung
- viele aufgrund von Sequenzvergleichen identifizierte Verwandtschaftsgruppen (Kladen) erstrecken sich über mehrere Baltimore-Gruppen. Unter den ersten solchen vom ICTV bestätigten Taxa waren
- die Ortervirales (Baltimore 6 und 7) – revers transkribierende RNA- und DNA-Viren: Retroviren und Pararetroviren. Es handelt sich um RNA-Viren mit DNA-Zwischenstadium bzw. umgekehrt.
- die Pleolipoviridae (Baltimore 1 und 2) – Vertreter mit dsDNA und Vertreter mit ssDNA
- bei den Bacilladnaviridae (ssDNA) gibt es kleine, lineare ssDNA-Fragmente, die komplementär sind zu Abschnitten des großen, zirkulären ssDNA-Genoms. Durch deren Anlagerung entsteht ein zirkuläres DNA-Genom, das in kurzen Abschnitten dsDNA, ansonsten ssDNA ist.
- die Endornaviridae sind (+)ssRNA-Viren (nach ICTV, das ist Baltimore 4), aber mit dsRNA-Zwischenstadium (Baltimore 3), meist wird letzteres isoliert. Daher werden sie verschiedentlich auch als dsRNA-Viren klassifiziert.[8]
- Im Übrigen wird schon nach Baltimore bei Einzelstrang-DNA-Viren nicht zwischen den beiden Polaritäten unterschieden, nur bei Einzelstrang-RNA-Viren. Grund ist, dass es bei ersteren keine klare Unterscheidbarkeit gibt.
DNA-Viren
DNA-Viren bilden keine taxonomische Verwandtschaftsgruppe (Klade), stattdessen ist dieser Begriff lediglich eine Sammelbezeichnung der Virusklassifikation. Unter den DNA-Viren konnten jedoch eine Reihe von Taxa (Ordnungen und höher) als Verwandtschaftsgruppen ausgemacht und vom ICTV bestätigt werden.
Baltimore-Gruppe I
Doppelstrang-DNA – dsDNA (englisch double strand), normale Genom-Form allen Lebens.[9]
- Reich Zilligvirae
- Phylum Taleaviricota
- Klasse Tokiviricetes
- Ordnung Ligamenvirales
- Ordnung Primavirales mit Familie Tristromaviridae
- zum Reich Bamfordvirae
- Phylum Nucleocytoviricota (veraltet „Nucleocytoplasmaviricota“, „Nucleocytoplasmic large DNA viruses“, NCLDV)
- Klasse Megaviricetes
- Zweig 1:
- Zweig 2:
- Ordnung Pimascovirales (früher „MAPI-Superklade“[12] oder „PMI-Gruppe“)
- Familien Marseilleviridae, Ascoviridae, Iridoviridae, evtl. „Mininucleoviridae“, „Pithoviridae“, sowie Gattung Ichnovirus aus Polydnaviridae
- Klasse Pokkesviricetes
- Zweig 3:
- Ordnung Asfuvirales, evtl. mit Gattung Dinodnavirus
- Ordnung Chitovirales (mit den Pockenviren)
- Phylum Preplasmiviricota
- Klasse Tectiliviricetes
- Ordnung Rowavirales (mit Adenoviren)
- Ordnung Kalamavirales
- Ordnung Vinavirales
- Ordnung Belfryvirales (mit Turriviridae)[14] (mit Gattung Alphaturrivirus,[15] dazu Spezies Sulfolobus turreted icosahedral virus 1 und 2, STIV1 und STIV2)
- ohne Ordnungszuweisung
- Familie Autolykiviridae
- Klasse Maveriviricetes
- Ordnung Priklausovirales (mit Virophagen der Lavidaviridae)
- Reich Helvetiavirae[11]
- Phylum Dividoviricota
- Klasse Laserviricetes
- Ordnung Halopanivirales (mit Sphaerolipoviridae)
- ohne Zuordnung zu einer Ordnung, Klasse, Phylum
- Familie Portogloboviridae (gemäß Vorschlag)
- Reich Heunggongvirae
- Phylum Uroviricota
- Klasse Caudoviricetes
- Ordnung Caudovirales (Bakteriophagen etc. mit Kopf-Schwanz-Struktur)
- Phylum Peploviricota
- Klasse Herviviricetes
- Ordnung Herpesvirales
- Reich Shotokuvirae (hier nur Vertreter mit dsDNA: Papovaviricetes)
- Phylum Cossaviricota (dito)
- Klasse Papovaviricetes
- weitere mögliche Kandidaten für diese Gruppe sind die folgenden dsDNA-Virusfamilen:
- in keinen höheren Rang klassifizierte Klasse:
- Klasse Naldaviricetes (ehemals „Modul 6“) mit folgenden Familien nach Vorschlag von Koonin et al. (2015, 2019)[20][21][22]
- Ordnung Lefavirales
- Familie Baculoviridae
- Familie Hytrosaviridae
- Familie Nudiviridae
- Ordnung nicht zugewiesen
- Familie Nimaviridae
- bisher nicht vom ICTV bestätigter Vorschlag
- Familie Polydnaviridae (vermutlich polyphyletisch,[23] hier nur Gattung Bracovirus)
- in keinen höheren Rang klassifizierte Familien:
- Familie Ampullaviridae
- Familie Bicaudaviridae
- Familie Clavaviridae
- Familie Fuselloviridae
- Familie Globuloviridae
- Familie Guttaviridae
- Familie Ovaliviridae
- Familie Plasmaviridae
- Familie Polydnaviridae (möglicherweise polyphyletisch, Bracovirus, Ichnovirus ( NCLDV, vermutlich eine gemeinsame Klade mit Ascoviridae und Iridoviridae zu Pimascovirales in Nucleocytoviricota))
- Familie Portogloboviridae
- Familie Thaspiviridae
- Familie Halspiviridae
- in keinen höheren Rang klassifizierte Gattungen:
- in keinen höheren Rang klassifizierte Spezies:
Baltimore-Gruppe II
Einzelstrang-DNA – ssDNA (englisch single strand). Virionen enthalten DNA positiver oder negativer Polarität.[31] Die Virusgruppe „CRESS“ (circular Rep-encoding single-strand DNA viruses) (im weiteren Sinne) ist keine Verwandtschaftsgruppe (Taxon), sondern polyphyletisch.[32][33][34][35][36] Das neue Phylum Cressdnaviricota fasst jedoch die hauptsächlichen Vertreter dieser in einer Verwandtschaftsgruppe zusammen.
- Reich Loebvirae
- Phylum Hofneiviricota
- Klasse Faserviricetes (filamentös)
- Ordnung Tubulavirales (zu „CRESS“)
- Familie Inoviridae
- Familie Paulinoviridae
- Familie Plectroviridae
- Reich Sangervirae
- Phylum Phixviricota
- Klasse Malgrandaviricetes
- Ordnung Petitvirales (mit Microviridae, zu „CRESS“ – circular Rep-encoding single-strand DNA viruses)
- Reich Shotokuvirae
- Phylum Cossaviricota (ohne Papovaviricetes da jene mit zirkulärer dsDNA)
- Klasse Quintoviricetes (mit Parvoviridae, zu „CRESS“)
- Klasse Mouviricetes (mit Bidnaviridae)
- Phylum Cressdnaviricota
- Klasse Repensiviricetes
- Ordnung Geplafuvirales (mit Geminiviridae und Genomoviridae)
- Klasse Arfiviricetes
- Ordnung Baphyvirales (mit Bacilladnaviridae)
- Ordnung Recrevirales (mit Redondoviridae)
- Ordnung Cirlivirales (mit Circoviridae)
- Ordnung Cremevirales (mit Smacoviridae)
- Ordnung Mulpavirales (mit Metaxyviridae und Nanoviridae)
- Ordnung Recrevirales(mit Redondoviridae, ssDNA)
- ohne Zuordnung zu einer Klasse oder Ordnung:
- Familie „Cruciviridae“ (Vorschlag)
- keinem höheren Rang zugeordnete Familien:
- Familie Spiraviridae ssDNA(+)
- Familie Anelloviridae ssDNA(-)
- Familie Finnlakeviridae ssDNA
- keinem höheren Rang zugeordnete vorgeschlagene Kladen (Gattungen?):
- Klade „Circularisvirus“[37]
- Spezies: „Dragonfly circularisvirus“ (DfCirV)[38] (zu „CRESS2“[39])
- Spezies: „Cybaeus spider associated circular virus 1“ (CySACV-1), in Spinnen der Gattung Cybaeus[40]
- Spezies: „Golden silk orbweaver associated circular virus 1“ (GoSOrbACV-1), in Spinnen der Gattung Nephila[40]
- Spezies: „Longjawed orbweaver circular virus 1“ (LjOrbCV-1), in Spinnen der Gattung Leucauge[40]
- Spezies: „Spinybacked orbweaver circular virus 1“ (SpOrbCV-1), in Spinnen der Gattung Gasteracantha[40]
- Klade „Volvovirus“[41]
- keinem höheren Rang zugeordnete vorgeschlagene Spezies:
Pleolipoviridae
Die Familie Pleolipoviridae war (mit der Ordnung Ortervirales) eines der ersten vom ICTV anerkannten Taxa (Verwandtschaftsgruppe, ermittelt nach der Genom-Sequenz), dessen Mitglieder in verschiedenen Baltimore-Gruppen (nämlich 1 und 2) fallen.
RNA-Viren
Im Wesentlichen identisch mit dem Realm Riboviria. Dazu gehören auch die vorgeschlagenen Supergruppen
- „Picornavirus-like superfamily“
- „Alphavirus-like superfamily“
nach Koonin et al. (2015), die Kladen verschiedener Baltimore-Gruppen zusammenfassen.
Baltimore-Gruppe III
Doppelstrang-RNA – dsRNA[49]
- zum Realm Riboviria (hier nur dsRNA)
- zum Reich Orthornavirae
- zum Phylum Pisuviricota
- zur Klasse Duplopiviricetes
- zur Ordnung Durnavirales (hier nur dsRNA-Viren)
- Familie Amalgaviridae
- Familie Partitiviridae (mit den Gattungen Alphapartitivirus, Betapartitivirus, Gammapartitivirus, Deltapartitivirus, Cryspovirus)
- Familie Picobirnaviridae (mit Gattung Picobirnavirus)
- zum Phylum Duplornaviricota
- zur Klasse Chrymotiviricetes
- zur Ordnung Ghabrivirales
- Familie Chrysoviridae (mit Gattung Alphachrysovirus, sowie Betachrysovirus7,[50] mit Spezies Colletotrichum fructicola chrysovirus 1)
- Familie Megabirnaviridae (mit Gattung Megabirnavirus)
- Familie Quadriviridae (mit Gattung Quadrivirus)
- Familie Totiviridae
- zur Klasse Vidaverviricetes
- Ordnung Mindivirales (mit Familie Cystoviridae)
- zur Klasse Resentoviricetes
- Ordnung Reovirales (mit Familie Reoviridae, nach Vorschlag Koonin et al. (2015) von den Cystoviridae abstammend)
- zum Phylum Kitrinoviricota
- zur Klasse Alsuviricetes
- zur Ordnung Martellivirales
- Familie Endornaviridae
- innerhalb der Orthornavirae keinem höheren Rang zugeordnet ist die Familie:
- Familie Birnaviridae
- innerhalb der Orthornavirae keinem höheren Rang zugeordnet ist die Gattung:
- Gattung Botybirnavirus
- innerhalb der Riboviria keinem höheren Rang zugeordnetdind die vorgeschlagenen Spezies:
Baltimore-Gruppe IV
Positive Einzelstrang-RNA – ss(+)RNA. Sie wirkt direkt als mRNA.[57]
- zum Realm Riboviria (hier nur ss(+)RNA)
- zum Reich Orthornavirae − hier nur ss(+)RNA
- Phylum Pisuviricota
- Klasse Pisoniviricetes
- Ordnung Nidovirales
- Ordnung Picornavirales
- Ordnung Sobelivirales (mit den Familien Barnaviridae, Alvernaviridae, Solemoviridae)
- Klasse Stelpaviricetes
- Ordnung Stellavirales (mit Familie Astroviridae, diese mit Gattung Mamastrovirus)
- Ordnung Patatavirales4(mit Familie Potyviridae)
- Klasse Duplopiviricetes
- Ordnung Durnavirales
- Phylum Kitrinoviricota
- Klasse Alsuviricetes
- Ordnung Tymovirales
- Ordnung Hepelivirales (mit den Familie Hepeviridae, Alphatetraviridae, Benyviridae, Matonaviridae – letztere mit Rötelnvirus)
- Ordnung Martellivirales
- Klasse Flasuviricetes
- Ordnung Amarillovirales (mit Familie Flaviviridae)
- Klasse Tolucaviricetes
- Ordnung Tolivirales (mit den Familien Luteoviridae, Carmotetraviridae, Tombusviridae)
- Klasse Magsaviricetes
- Ordnung Nodamuvirales
- Phylum Lenarviricota
- Klasse Allassoviricetes
- Ordnung Levivirales (mit Familie Leviviridae)
- keinem höheren Rang unter Orthornaviae zugeteilt:
- Familie Permutotetraviridae
- keinem Realm zugeteilt:
- Spezies „Yellowstone hot spring archaeal RNA virus“ mit ca. drei Viren(stämmen): Contig1 bis 9 (Vorschlag, evtl. mehrere Spezies?) – Wirt(e): Sulfolobales-Spezies (Archaeen), Fundort: sauer-heiße Quelle NL10 am Nymph Lake[A. 1] im Yellowstone-Nationalpark, Genom: ssRNA positiver Polarität, d. h. ss(+)RNA: Baltimore-Gruppe IV.[60][61][62]
Baltimore-Gruppe V
Negative Einzelstrang-RNA – ss(-)RNA. Sie wirkt als Matrize zur mRNA Synthese.[63]
- zum Realm Riboviria (hier nur ss(-)RNA)
- Realm Ribozyviria – ss(-)RNA.
- Phylum, Subphylum, Klasse, Ordnung nicht bestimmt bei:
- Familie: Kolmioviridae (mit Gattung Deltavirus)
Revers transkribierende Viren
Dazu gehören Viren mit positiver Einzelstrang-RNA, die per Reverse Transkriptase (RT) in DNA zurückgeschrieben und ins Zellgenom eingebaut wird (Retroviren ssRNA-RT, Baltimore-Gruppe 6), sowie Viren mit Doppelstrang-DNA, die umgekehrt zur Replikation einen RNA-Zwischenschritt benutzen und daher ebenfalls revers transkribieren (Pararetroviren dsDNA-RT, Baltimore-Gruppe 7). Die meisten dieser Vertreter gehören unabhängig davon der Ordnung Ortervirales an.[64]
Baltimore-Gruppe VI
Positive Einzelstrang-RNA, die per Reverse Transkriptase (RT) in DNA zurückgeschrieben und ins Zellgenom eingebaut wird (Retroviren).
- zum Realm Riboviria
- zur Ordnung Ortervirales (hier bis auf Caulimoviridae - revers transkribierende RNA-Viren ssRNA-RT)
Baltimore-Gruppe VII
Doppelstrang-DNA, die zur Replikation einen RNA-Zwischenschritt benutzt (revers transkribierende DNA-Viren dsDNA-RT, Pararetroviren).
- zum Realm Riboviria
- zur Ordnung Ortervirales (hier nur Sonderfall Caulimoviridae ssDNA-RT)
- Familie Caulimoviridae (dsDNA-RT: Revers transkribierende DNA-Viren)
- Ordnung Blubervirales (dsDNA-RT: Revers transkribierende DNA-Viren, mit Hepadnaviridae)
Tabellarische Übersicht
| Nukleinsäure | Kapsidsymmetrie | Hülle | Genom | Baltimore-Klasse | Familie | Genus | Arten |
|---|---|---|---|---|---|---|---|
| DNA | ikosaedrisch | umhüllt | ds | VII | Hepadnaviridae | Orthohepadnavirus | Hepatitis-B-Virus |
| DNA | ikosaedrisch | umhüllt | ds | I | Herpesviridae | Simplexvirus | Herpes-simplex-Virus 1 und 2 |
| RNA | ikosaedrisch | umhüllt | ss(+) | IV | Flaviviridae | Flavivirus | Gelbfieber-Virus, Hepatitis-C-Virus |
| RNA | komplex | umhüllt | ss(+) | VI | Retroviridae | Lentivirus | HIV-1,-2, SIV |
Weblinks
Anmerkungen
- ↑ Die Koordinaten der saueren Thermalquelle NL10 geben Wang et al. (2015) als
 ♁44,7535° N, 110,7238° W an.
♁44,7535° N, 110,7238° W an.
Einzelnachweise
- ↑ Francesco Fiume: Viruses, §LHT System of Virus Classification (Letzte Aktualisierung: 2005).
- ↑ International Committee on Taxonomy of Viruses Executive Committe,
Virus Taxonomy: 2024 Release,
 How to write virus and species names
How to write virus and species names
- ↑ International Committee on Taxonomy of Viruses Executive Committee:
The new scope of virus taxonomy: partitioning the virosphere into 15 hierarchical ranks, in: Nature Microbiology Band 5, S. 668–674
vom 27. April 2020,
 doi:10.1038/s41564-020-0709-x; sowie Nadja Podbregar:
doi:10.1038/s41564-020-0709-x; sowie Nadja Podbregar:
 Ein Stammbaum für die Virosphäre, auf: scinexx.de vom 29. April 2020. Beide Artikel haben inhaltlich den
Stand von Januar 2020, d. h. Einzelheiten der Master Species List (MSL) Nr. 35 des ICTV vom März 2020 sind noch nicht alle berücksichtigt. Für die grundsätzliche Intention des ICTV hat das aber keine Bedeutung,
die Entwicklung ist mit der MSL#35 lediglich in der vorgegebenen Richtung schon wieder weitergegangen.
Ein Stammbaum für die Virosphäre, auf: scinexx.de vom 29. April 2020. Beide Artikel haben inhaltlich den
Stand von Januar 2020, d. h. Einzelheiten der Master Species List (MSL) Nr. 35 des ICTV vom März 2020 sind noch nicht alle berücksichtigt. Für die grundsätzliche Intention des ICTV hat das aber keine Bedeutung,
die Entwicklung ist mit der MSL#35 lediglich in der vorgegebenen Richtung schon wieder weitergegangen.
- ↑
 ICTV 2024 Master Species List (MSL40)
ICTV 2024 Master Species List (MSL40)
- ↑ Lars Gerdes, Ulrich Busch, Sven Pecoraro:
 Parallele Quantifizierung von gentechnisch veränderten Organismen (GVO),
in: Schriftenreihe Gentechnik für Umwelt und Verbraucherschutz, Band 8, 5. Fachtagung "Gentechnik für Umwelt- und Verbraucherschutz", Oberschleißheim, November 2013: Conference Paper, hier: Abb. 6.1:
Parallele Quantifizierung von gentechnisch veränderten Organismen (GVO),
in: Schriftenreihe Gentechnik für Umwelt und Verbraucherschutz, Band 8, 5. Fachtagung "Gentechnik für Umwelt- und Verbraucherschutz", Oberschleißheim, November 2013: Conference Paper, hier: Abb. 6.1:
 Baltimore-Klassifikation und Virusfamilien
Baltimore-Klassifikation und Virusfamilien
- ↑ D. Sander: Family Groups - The Baltimore Method, The Big Picture Book of Viruses, Garry Lab, 1995–2007
- ↑ SIB:
 Baltimore classification, auf: ViralZone
Baltimore classification, auf: ViralZone
- ↑ SIB:
 Endornaviridae
Endornaviridae
- ↑ SIB:
 Double Strand DNA Viruses, auf: ViralZone
Double Strand DNA Viruses, auf: ViralZone
- ↑ Eugene V. Koonin, Valerian V. Dolja, Mart Krupovic, Arvind Varsani, Y. I. Wolf, Natalya Yutin, M. Zerbini, Jens H. Kuhn: Create a megataxonomic framework for DNA viruses encoding vertical jelly roll-type major capsid proteins filling all principal taxonomic ranks (vom 17. März 2020)
- ↑ Hochspringen nach: a b c ICTV Master Species List 2019 v1 MSL #35, März 2019
- ↑ Hochspringen nach: a b Julien Guglielmini, Anthony C. Woo, Mart Krupovic,
Patrick Forterre, Morgan Gaia:
 Diversification of giant and large eukaryotic dsDNnA viruses predated the origin of modern eukaryotes,
in: PNAS, Band 116, Nr. 39, 10./24. September 2019, S. 19585–19592,
Diversification of giant and large eukaryotic dsDNnA viruses predated the origin of modern eukaryotes,
in: PNAS, Band 116, Nr. 39, 10./24. September 2019, S. 19585–19592,
 doi:10.1073/pnas.1912006116,
doi:10.1073/pnas.1912006116,
 PMID 31506349.
PMID 31506349.
Julien Guglielmini, Anthony Woo, Mart Krupovic, Patrick Forterre, Morgan Gaia: Diversification of giant and large eukaryotic dsDNA viruses predated the origin of modern eukaryotes, auf: bioRxiv vom 29. Oktober 2018, doi:10.1101/455816. bioRxiv:
doi:10.1101/455816. bioRxiv:
 10.1101/455816v1 (Preprint-Volltext) (PrePrint).
10.1101/455816v1 (Preprint-Volltext) (PrePrint).
- ↑ Sailen Barik:
 A Family of Novel Cyclophilins, Conserved in the Mimivirus Genus of the Giant DNA Viruses, in:
Computational and Structural Biotechnology Journal, Band 16, Juli 2018, S. 231–236,
A Family of Novel Cyclophilins, Conserved in the Mimivirus Genus of the Giant DNA Viruses, in:
Computational and Structural Biotechnology Journal, Band 16, Juli 2018, S. 231–236,
 doi:10.1016/j.csbj.2018.07.001
doi:10.1016/j.csbj.2018.07.001
- ↑ SIB:
 Turriviridae, auf: ViralZone
Turriviridae, auf: ViralZone
- ↑ SIB:
 Alphaturrivirus, auf: ViralZone
Alphaturrivirus, auf: ViralZone
- ↑ Nicole L. Welch, Natalya Yutin et al.: Adomaviruses: an emerging virus family provides insights into DNA virus evolution,
in: bioRxiv, 7. Juni 2018 bioRxiv:
 2018/06/07/341131
(Preprint-Volltext),
doi:10.1101/341131, insbes. Fig. 7
2018/06/07/341131
(Preprint-Volltext),
doi:10.1101/341131, insbes. Fig. 7
- ↑ Hochspringen nach: a b Nicole L. Welch, Michael J. Tisza et al.:
Identification of “Missing Link” Families of Small DNA Tumor Viruses, in: BioRxiv; Cold Spring Harbor, 11. Juli 2019, bioRxiv:
 10.1101/697771v3 (Preprint-Volltext)
10.1101/697771v3 (Preprint-Volltext)
- ↑ NCBI:
 Adomaviridae (family)
Adomaviridae (family)
- ↑ NCBI:
 Adintoviridae (family)
Adintoviridae (family)
- ↑ Eugene V. Koonin, Natalya Yutin:
 Evolution of the Large Nucleocytoplasmatic DNA Viruses of Eukaryotes and Convergent Origins of Viral Gigantism,
in: Advances in Virus research, Band 103, AP 21. Januar 2019,
Evolution of the Large Nucleocytoplasmatic DNA Viruses of Eukaryotes and Convergent Origins of Viral Gigantism,
in: Advances in Virus research, Band 103, AP 21. Januar 2019,
 doi:10.1016/bs.aivir.2018.09.002, S. 167–202.
doi:10.1016/bs.aivir.2018.09.002, S. 167–202.
- ↑ Hochspringen nach: a b Eugene V. Koonin, Valerian V. Dolja,
Mart Krupovic: Origins and evolution of viruses of eukaryotes: The ultimate modularity, in: Virology Mai 2015; 479–480. 2–25.
 PMC 5898234 (freier Volltext),
PMC 5898234 (freier Volltext),
 PMID 25771806
PMID 25771806
- ↑ Jaime Iranzo, Mart Krupovic, Eugene V. Koonin: The Double-Stranded DNA Virosphere as a Modular Hierarchical Network of Gene Sharing,
in: mBio 7(4), Juli–August 2016, e00978-16,
 doi:10.1128/mBio.00978-16,
doi:10.1128/mBio.00978-16,
 PMC 4981718 (freier Volltext),
PMC 4981718 (freier Volltext),
 PMID 27486193
PMID 27486193
- ↑ Dupuy C, Huguet E, Drezen JM: Unfolding the evolutionary
story of polydnaviruses. In: Virus Res. 117. Jahrgang, Nr. 1, 2006,
S. 81–89,
doi:
 10.1016/j.virusres.2006.01.001,
10.1016/j.virusres.2006.01.001,
 PMID 16460826.
PMID 16460826.
- ↑ H. Ogata, K. Toyoda, Y. Tomaru, N. Nakayama, Y. Shirai, J. M. Claverie, K. Nagasaki:
 Remarkable sequence similarity between the dinoflagellate-infecting marine girus and the terrestrial pathogen
African swine fever virus. In: Virol J. 6, 2009, S. 178.
Remarkable sequence similarity between the dinoflagellate-infecting marine girus and the terrestrial pathogen
African swine fever virus. In: Virol J. 6, 2009, S. 178.
- ↑ SIB:
 Rhizidiovirus, auf: ViralZone.
Rhizidiovirus, auf: ViralZone.
- ↑ NCBI:
 Tetraselmis viridis virus N1 (species)
Tetraselmis viridis virus N1 (species)
- ↑ Hochspringen nach: a b António Pagarete, Théophile Grébert, Olga Stepanova, Ruth-Anne Sandaa,
Gunnar Bratbak:
 TsV-N1: A Novel DNA Algal Virus that Infects Tetraselmis striata, in: MDPI Viruses, Band 7, Nr. 7, Section Viruses of Plants,
Fungi and Protozoa, 17. Juli 2015, S. 3937–3953,
TsV-N1: A Novel DNA Algal Virus that Infects Tetraselmis striata, in: MDPI Viruses, Band 7, Nr. 7, Section Viruses of Plants,
Fungi and Protozoa, 17. Juli 2015, S. 3937–3953,
 doi:10.3390/v7072806
doi:10.3390/v7072806
- ↑ Christopher M. Bellas, Ruben Sommaruga:
 Polinton-like viruses and virophages are widespread in aquatic ecosystems, auf:
Cold Spring Harbor Laboratory bioRxiv vom 13. Dezember 2019,
Polinton-like viruses and virophages are widespread in aquatic ecosystems, auf:
Cold Spring Harbor Laboratory bioRxiv vom 13. Dezember 2019,
 doi:10.1186/s40168-020-00956-0
doi:10.1186/s40168-020-00956-0
- ↑ Janice E. Lawrence, Amy M. Chan, Curtis A. Suttle: A novel virus (HaNIV) causes lysis of the toxic bloom-forming alga Heterosigma
akashiwo (Raphidophyceae), in: Journal of Phycology, Band 37, Nr. 2, April 2001, Epub 1. Mai 2002, S. 216–222,
 doi:10.1046/j.1529-8817.2001.037002216.x
doi:10.1046/j.1529-8817.2001.037002216.x
- ↑ Janice E. Lawrence, Corina P. D. Brussaard, Curtis A. Suttle: Virus-Specific Responses of Heterosigma akashiwo to Infection, in: Appl Environ Microbiol.,
Dezember 2006 Dec, Band 72, Nr. 12, 7S. 829–7834, Epub 23. Oktober 2006,
 doi:10.1128/AEM.01207-06,
doi:10.1128/AEM.01207-06,
 PMID 17041155,
PMID 17041155,
 PMC 1694243 (freier Volltext).
PMC 1694243 (freier Volltext).
- ↑ SIB:
 Single Strand DNA Viruses, auf: ViralZone
Single Strand DNA Viruses, auf: ViralZone
- ↑ Mart Krupovic:
 Networks of evolutionary interactions underlying the polyphyletic origin of ssDNA viruses,
in: Current Opinion in Virology Band 3, Nr. 5, Oktober 2013, S. 578–586,
Networks of evolutionary interactions underlying the polyphyletic origin of ssDNA viruses,
in: Current Opinion in Virology Band 3, Nr. 5, Oktober 2013, S. 578–586,
 doi:10.1016/j.coviro.2013.06.010,
doi:10.1016/j.coviro.2013.06.010,
 PMID 23850154
PMID 23850154
- ↑ Karyna Rosario, Siobain Duffy, Mya Breitbart: A field guide to eukaryotic circular single-stranded DNA viruses: insights gained
from metagenomics. In: Archives of Virology. 157. Jahrgang, Nr. 10, Oktober 2012,
S. 1851–1871,
doi:
 10.1007/s00705-012-1391-y,
10.1007/s00705-012-1391-y,
 PMID 22760663.
PMID 22760663.
- ↑ Darius Kazlauskas, Arvind Varsani, Eugene V. Koonin, Mart Krupovic: Multiple origins of prokaryotic and eukaryotic single-stranded
DNA viruses from bacterial and archaeal plasmids. In: Nature Communications. 10. Jahrgang,
Nr. 1, 2019, S. 3425,
doi:
 10.1038/s41467-019-11433-0
(
10.1038/s41467-019-11433-0
(  nature.com).
nature.com).
- ↑ NCBI:
 CRESS viruses
CRESS viruses
- ↑ Richard Harth:
 Major class of viruses reveals complex origins,
auf: ScienceDaily: Science News, 31. Juli 2019, Arizona State University
Major class of viruses reveals complex origins,
auf: ScienceDaily: Science News, 31. Juli 2019, Arizona State University
- ↑ NCBI:
 Circularisvirus (clade)
Circularisvirus (clade)
- ↑ Hochspringen nach: a b c Karyna Rosario,
Anisha Dayaram, Milen Marinov, Jessica Ware, Simona Kraberger, Daisy Stainton, Mya Breitbart, Arvind Varsani:
 Diverse circular ssDNA viruses discovered in dragonflies (Odonata: Epiprocta),
in: Journal of General Virology Band 93, Nr. 12, 1. Dezember 2012,
Diverse circular ssDNA viruses discovered in dragonflies (Odonata: Epiprocta),
in: Journal of General Virology Band 93, Nr. 12, 1. Dezember 2012,
 doi:10.1099/vir.0.045948-0. Insbes.
doi:10.1099/vir.0.045948-0. Insbes.
 Tbl. 2
Tbl. 2
- ↑ Hochspringen nach: a b c
d Darius Kazlauskas, Arvind Varsani, Mart Krupovic:
Pervasive Chimerism in the Replication-Associated Proteins of Uncultured Single-Stranded DNA Viruses, in: MDPI Viruses, Band 10, Nr. 4,
Special Issue Viral Recombination: Ecology, Evolution and Pathogenesis, 10. April 2018, 187,
 doi:10.3390/v10040187; siehe Excel-Datei in
doi:10.3390/v10040187; siehe Excel-Datei in
 Supplement S1 (ZIP: pdf, xlsx, auto. Download)
Supplement S1 (ZIP: pdf, xlsx, auto. Download)
- ↑ Hochspringen nach: a b c
d e Karyna Rosario, Kaitlin Mettel, Bayleigh Benner, Ryan Johnson, Catherine Scott, Sohath Yusseff-Vanegas, Christopher Baker,
Deby Cassill, Caroline Storer, Arvind Varsani, Mya Breitbart:
 Virus Discovery in All Three Major Lineages of Terrestrial Arthropods Highlights the
Diversity of Single-stranded DNA Viruses Associated with Invertebrates, University of South Florida, College of Marine Science: Scholar Commons — Marine Science Faculty Publications, 2017,
Virus Discovery in All Three Major Lineages of Terrestrial Arthropods Highlights the
Diversity of Single-stranded DNA Viruses Associated with Invertebrates, University of South Florida, College of Marine Science: Scholar Commons — Marine Science Faculty Publications, 2017,
 652. Part of the Life Sciences Commons. 11. Oktober 2018
652. Part of the Life Sciences Commons. 11. Oktober 2018
 PeerJ,
PeerJ,
 PMID 30324030,
PMID 30324030,
 PMC 6186406 (freier Volltext),
PMC 6186406 (freier Volltext),
 doi:10.7717/peerj.5761
doi:10.7717/peerj.5761
- ↑ NCBI:
 Volvovirus (clade)
Volvovirus (clade)
- ↑ Hanh T. Pham, Max Bergoin, Peter Tijssen: Acheta domesticus Volvovirus, a Novel Single-Stranded Circular DNA Virus of the House Cricket, in: Genome Announc. 1(2),
März-April 2013, e00079-13. Epub 14. März 2013,
 doi: 10.1128/genomeA.00079-13,
doi: 10.1128/genomeA.00079-13,
 PMID 23516206,
PMID 23516206,
 PMC 3623006 (freier Volltext).
PMC 3623006 (freier Volltext).
- ↑ Hanh T. Pham, Hajime Iwao, Max Bergoin, Peter Tijssen: New Volvovirus Isolates from Acheta domesticus (Japan) and Gryllus assimilis (United States),
in: ASM Journals: Genome Announcements, Band 1, Nr. 3, 6. Juni 2013,
 doi:10.1128/genomeA.00328-13
doi:10.1128/genomeA.00328-13
- ↑ NCBI:
 Dragonfly orbiculatusvirus (species)
Dragonfly orbiculatusvirus (species)
- ↑ NCBI:
 Dragonfly cyclicusvirus (species)
Dragonfly cyclicusvirus (species)
- ↑ Sencilo A, Paulin L, Kellner S, Helm M, Roine E: Related haloarchaeal pleomorphic viruses contain different genome types.
In: Nucleic Acids Research. 40. Jahrgang, Nr. 12, Juli 2012,
S. 5523–34,
doi:
 10.1093/nar/gks215,
10.1093/nar/gks215,
 PMID 22396526,
PMID 22396526,
 PMC 3384331 (freier Volltext).
PMC 3384331 (freier Volltext).
- ↑ Maija K. Pietilä, Elina Roine, Ana Sencilo, Dennis H. Bamford, Hanna M. Oksanen: Pleolipoviridae, a
newly proposed family comprising archaeal pleomorphic viruses with single-stranded or double-stranded DNA genomes. In: Archives of Virology. 161. Jahrgang,
Nr. 1, Januar 2016, S. 249–56,
doi:
 10.1007/s00705-015-2613-x,
10.1007/s00705-015-2613-x,
 PMID 26459284.
PMID 26459284.
- ↑ Maija K. Pietilä, Nina S. Atanasova, Violeta Manole, Lassi Liljeroos, Sarah J. Butcher, Hanna M. Oksanen, Dennis H. Bamford:
Virion architecture unifies globally distributed pleolipoviruses infecting halophilic archaea. In: Journal of Virology. 86. Jahrgang,
Nr. 9, Mai 2012, S. 5067–79,
doi:
 10.1128/JVI.06915-11,
10.1128/JVI.06915-11,
 PMID 22357279,
PMID 22357279,
 PMC 3347350 (freier Volltext).
PMC 3347350 (freier Volltext).
- ↑ SIB:
 Double Strand RNA Viruses, auf: ViralZone
Double Strand RNA Viruses, auf: ViralZone
- ↑ SIB:
 Double Stranded RNA Viruses, auf: ViralZone
Double Stranded RNA Viruses, auf: ViralZone
- ↑
 Circulifer tenellus virus 1, auf: Virus-Host DB
Circulifer tenellus virus 1, auf: Virus-Host DB
- ↑ NCBI:
 Circulifer tenellus virus 1 (species)
Circulifer tenellus virus 1 (species)
- ↑ Henxia Xia et al.:
 A dsRNA virus with filamentous viral particled,
in: Nature Communicationsvolume 8, Nr. 168 (2017),
A dsRNA virus with filamentous viral particled,
in: Nature Communicationsvolume 8, Nr. 168 (2017),
 doi:10.1038/s41467-017-00237-9
doi:10.1038/s41467-017-00237-9
- ↑ NCBI:
 camelliae filamentous virus 1 (species)
camelliae filamentous virus 1 (species)
- ↑
 Spissistilus festinus virus 1, auf: Virus-Host DB
Spissistilus festinus virus 1, auf: Virus-Host DB
- ↑ NCBI:
 Spissistilus festinus virus 1 (species)
Spissistilus festinus virus 1 (species)
- ↑ SIB:
 Positive Strand RNA Viruses, auf: ViralZone
Positive Strand RNA Viruses, auf: ViralZone
- ↑ ICTV:
 Sarthroviridae
(vom 22. September 2020 im Internet Archive)
Sarthroviridae
(vom 22. September 2020 im Internet Archive)
- ↑ SIB:
 Macronovirus, auf: ExPASy: ViralZone
Macronovirus, auf: ExPASy: ViralZone
- ↑ NCBI Taxonomy Browser:
 Yellowstone hot spring archaeal RNA virus (species), Nucleotide:
Yellowstone hot spring archaeal RNA virus (species), Nucleotide:
 Yellowstone hot spring archaeal RNA virus genomic RNA.
Yellowstone hot spring archaeal RNA virus genomic RNA.
- ↑ Benjamin Bolduc, Daniel P. Shaughnessy, Yuri I. Wolf, Eugene V. Koonin, Francisco F. Roberto, Mark Young: Identification of Novel
Positive-Strand RNA Viruses by Metagenomic Analysis of Archaea-Dominated Yellowstone Hot Springs. In: ASM Journals: Journal of Virology, Band 86, Nr. 10;
 doi:10.1128/JVI.07196-11.
doi:10.1128/JVI.07196-11.
- ↑ Hongming Wang, Yongxin Yu, Taigang Liu, Yingjie Pan, Shuling Yan, Yongjie Wang: Diversity of putative archaeal RNA viruses in metagenomic
datasets of a yellowstone acidic hot spring. In: SpringerPlus, Band 4, Nr. 189, 18. April 2015;
 doi:10.1186/s40064-015-0973-z.
doi:10.1186/s40064-015-0973-z.
- ↑ SIB:
 Negative Strand RNA Viruses, auf: ViralZone
Negative Strand RNA Viruses, auf: ViralZone
- ↑ SIB:
 Reverse Transcribing Viruses, auf: ViralZone
Reverse Transcribing Viruses, auf: ViralZone


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 06.04. 2026