Glas
Glas (von germanisch glasa "das Glänzende, Schimmernde", auch für "Bernstein") ist ein amorpher, nichtkristalliner Stoff. Materialien, die man im Alltagsleben als Glas bezeichnet (zum Beispiel Trink- und Fenstergläser, Flaschen und Glühlampen) sind nur ein Ausschnitt aus der Vielfalt der Gläser.

Versuch einer Definition
Nehmen wir die Eigenschaften des Glases, die wir vom alltäglichen Umgang mit ihm seit langem kennen: lichtdurchlässig; spröde, daher leicht zerbrechlich; bemerkenswert temperaturbeständig; ziemlich unempfindlich gegen Laugen, Säuren und andere Stoffe, also chemisch beständig - ein Begriff, der wohl den meisten von uns noch aus dem Chemieunterricht erinnerlich ist. Außerdem durften wir das Glas bislang mit ruhigem Gewissen zu den elektrischen Nichtleitern zählen, ohne daß uns jemand ernsthaft widersprochen hätte.
Eine "feste Flüssigkeit"
So weit, so gut. Läßt sich das Glas aber jetzt, nachdem uns seine wichtigsten Eigenschaften bekannt sind, näher beschreiben? Leider immer noch nicht, zumal heutzutage Eingeweihte verhalten lächeln, wenn wir die landläufigen Kenntnisse von den Eigenschaften des Glases zum besten geben. Ist doch inzwischen gut bekannt, daß sich die Strahlungsdurchlässigkeit des Glases über den sichtbaren Bereich des Spektrums hinaus für das ultraviolette und infrarote Licht erweitert hat, daß seine Festigkeit durch spezielle Behandlung wesentlich erhöht werden kann und dann Anwendungen ermöglicht, die noch vor wenigen Jahren undenkbar waren. Durch chemische Verfestigung beispielsweise werden bereits weitgehend bruchsichere Gebrauchsgläser angeboten, die sich unter großer Beanspruchung - etwa in Gaststätten und Hotels - bestens bewähren.
Auch hat man herausgefunden, daß Glas in bestimmter Zusammensetzung ionenleitend ist. Sein Einsatz als Halbleiter in der Elektrotechnik ist bereits weit verbreitet. Mit dem elektrischen Nichtleiter ist es demnach auch so eine Sache. Und erst recht mußten wir an der chemischen Beständigkeit des Glases zu zweifeln beginnen. Es hat sich nämlich herausgestellt, daß nicht wenige glaszerstörende Umwelteinflüsse wirken; daß Glas zum Beispiel von bestimmten alkalischen Lösungen deutlich angegriffen wird, ja, daß sogar Wasser Gläser bestimmter Zusammensetzung zerstören kann! In diesem Zusammenhang sei überhaupt darauf hingewiesen, daß Glas nicht immer gleich Glas ist. Die Wissenschaft beherrscht seine Eigenschaften und Verhaltensweisen heute so gut, daß es möglich ist, sie bewußt zu steuern. So kann man bei speziellen Glasarten auf bestimmte Eigenschaften - zum Beispiel optische - verzichten und dafür andere - zum Beispiel die Temperaturwechselbeständigkcit - stärker ausprägen.
- vergleiche hierzu: Glasarten, Glasgeschichte

© Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Ferner kommt technisch verwendbares Glas in der Natur nicht vor. Es ist immer Produkt menschlicher Arbeit, entstanden durch Mischen und Verarbeiten anderer Ausgangsstoffe. Dieses Glas ist stets ein von Menschen bewußt und künstlich hergestellter Stoff. Aber auch diese Feststellung hilft uns nicht wesentlich weiter, weil es für die Kennzeichnung vieler Stoffe recht unerheblich ist, ob sie in der Natur vorgefunden oder künstlich hergestellt werden. Für Diamanten beispielsweise gibt es bereits künstlich hergestellte Substitute (Fianit), die bei entsprechendem Schliff nicht einmal Fachleuten sofort als synthetisch erkennbar sind.
Worin aber liegt nun
endlich "des Pudels Kern"?
Was ist es, das den Charakter
des Glases ausmacht, was hat das Wesen dieses Stoffes bislang so
verborgen?
Es ist der innere
Aufbau, seine Struktur, die das Glas von der üblichen Materie
eindeutig unterscheidet: Wenn die Schmelze eines Stoffes
abkühlt, beginnt er von einem bestimmten Punkt an gewöhnlich
sehr schnell zu erstarren und - bei genauerer Untersuchung -
zu kristallisieren. Es bilden sich Kristalle, deren innere
Bausteine eine bestimmte, den erstarrten Stoff eindeutig
kennzeichnende Anordnung haben.
Bei zähflüssigen Schmelzen - zu vergleichen etwa mit dickflüssigem Bienenhonig - sind die inneren Transportvorgänge, die sich während des Erhitzens oder Erkaltens vollziehen, behindert, und mag es dabei vielleicht nur um die für den Kristallaufbau notwendige Drehung der Bausteine in eine Richtung gehen, damit sie zum Kristallbauwerk passen. In diesem Fall verläuft die Kristallisation relativ langsam. Bei ausreichend rascher Abkühlung ist es möglich, die Schmelze so erstarren zu lassen, daß sie nicht vollständig, unter Umständen gar nicht kristallisiert. Man sagt hierzu, daß die Temperaturgebiete der Kristallkeimbildung und des Kristallwachstums ausreichend schnell durchfahren werden müssen. Das Erstarrungsprodukt ist dann amorph, gestaltlos. Solche Stoffe nennt man Gläser. Der Vorgang ist, einfach ausgedrückt, folgender: Beim Abkühlen durchläuft die Glasschmelze einen Temperaturpunkt, bei dem sie eigentlich kristallisieren und in einen Festkörper übergehen müßte. Das tritt jedoch nicht ein, die Schmelze passiert einen sogenannten Transformationsbereich der Temperatur und erstarrt allmählich zu einem Festkörper, bei dem die Kristallisation ausgeblieben ist. Dieser Festkörper aus Glas ist ein zwar ziemlich formstabiler Stoff in festem Aggregatzustand, aber in Wirklichkeit ist er amorph geblieben wie die Flüssigkeit, aus der er erstarrte. "Flüssigkeit mit fixierter Struktur" ist daher eine treffende Bezeichnung für den Glaszustand mit spezifischen Eigenschaften. Weit verbreitet nennt man den beschriebenen Vorgang "Unterkühlung", und Glas wurde daher lange Zeit auch als "unterkühlte Flüssigkeit" bezeichnet.
Aus der Tatsache, ein nichtkristallisierter Festkörper zu sein, resultiert das prinzipiell unterschiedliche Schmelzverhalten des Glases gegenüber den Metallen und allen kristallinen Körpern, wie zum Beispiel auch Eis. Diese Körper bleiben während der Erwärmung zunächst im festen Aggregatzustand. Wenn die Schmelztemperatur, die beispielsweise bei Aluminium 660° C, bei Eis 0° C beträgt, erreicht ist, geht der feste Körper plötzlich in die flüssige Phase über. Gleiches vollzieht sich bei Abkühlung der Schmelze. Ist der Erstarrungspunkt erreicht, nimmt sie in der Regel sofort den festen Aggregatzustand an, sie kristallisiert und kühlt dann weiter ab.
 Ganz anders beim Glas. Ein Glasbrocken erweicht bei zunehmender Erhitzung. Er
verliert allmählich seine ursprüngliche Form und fließt
schließlich zu einer zähflüssigen Schmelze
auseinander, die bei weiterem Erhitzen "flüssiger", "dünner"
wird. Hier gibt es keinen plötzlichen Übergang vom festen
in den flüssigen Aggregatzustand, ein genau bestimmter
Schmelzpunkt läßt sich nicht angeben. Es gibt lediglich
einen Erweichungsbereich, der je nach Art des Glases recht
unterschiedlich ist.
In umgekehrter
Richtung ist der Vorgang der gleiche. Die dünne Glasschmelze
wird in einem bestimmten Erstarrungsbereich immer zähflüssiger,
bis sie schließlich wieder in den festen Aggregatzustand
übergeht, ohne dabei zu kristallisieren. Zugegeben, das alles
ist nicht ganz einfach zu verstehen. Aber diese Prozesse sind selbst
äußerst kompliziert und daher nun einmal auch nicht
leicht erklärbar. Sie verlangen schon ein wenig "Vertiefung
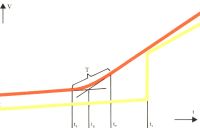
in die Materie". Die Abbildung
zeigen die Zustandsbereiche bei Glas und Kristallen in Abhängigkeit
von der Temperatur.
Ganz anders beim Glas. Ein Glasbrocken erweicht bei zunehmender Erhitzung. Er
verliert allmählich seine ursprüngliche Form und fließt
schließlich zu einer zähflüssigen Schmelze
auseinander, die bei weiterem Erhitzen "flüssiger", "dünner"
wird. Hier gibt es keinen plötzlichen Übergang vom festen
in den flüssigen Aggregatzustand, ein genau bestimmter
Schmelzpunkt läßt sich nicht angeben. Es gibt lediglich
einen Erweichungsbereich, der je nach Art des Glases recht
unterschiedlich ist.
In umgekehrter
Richtung ist der Vorgang der gleiche. Die dünne Glasschmelze
wird in einem bestimmten Erstarrungsbereich immer zähflüssiger,
bis sie schließlich wieder in den festen Aggregatzustand
übergeht, ohne dabei zu kristallisieren. Zugegeben, das alles
ist nicht ganz einfach zu verstehen. Aber diese Prozesse sind selbst
äußerst kompliziert und daher nun einmal auch nicht
leicht erklärbar. Sie verlangen schon ein wenig "Vertiefung
in die Materie". Die Abbildung
zeigen die Zustandsbereiche bei Glas und Kristallen in Abhängigkeit
von der Temperatur.
Als Grundlage dafür und als Ausgangspunkt für weitere Überlegungen mag die folgende zusammenfassende Definition des Glaszustandes dienen:
"Als Glas werden alle amorphen Körper bezeichnet, die man durch Unterkühlung einer Schmelze erhält, unabhängig von ihrer chemischen Zusammensetzung und dem Temperaturbereich ihrer Verfestigung, und die infolge der allmählichen Zunahme der Viskosität die mechanischen Eigenschaften fester Körper annehmen. Der Übergang aus dem flüssigen in den Glaszustand muß reversibel sein."
Natürlich gibt
es noch viele andere Versuche, den Glaszustand allgemein und speziell
zu definieren, und die Auffassungen hierzu sind bis heute nicht
ganz einheitlich. Das liegt wohl hauptsächlich daran, daß
der Zustand Glas noch lange nicht vollständig erforscht ist. Mit
neuen Forschungsergebnissen erschließen sich
verständlicherweise auch für den Stoff Glas immer neue
Einsatzgebiete.
So war von völlig
neuen Glasstrukturen jüngst aus Großbritannien zu hören.
Die erstaunlichen Neuentwicklungen bestehen aus Kalium-,
Natrium-
und Phosphoroxiden,
geschmolzen im Platintiegel bei 1.100 Grad
Celsius. Das stark wasserlösliche Glas enthält kein
Silizium (!), und seine Wasserlöslichkeit läßt sich auf jeden gewünschten Konzentrationsgrad einstellen. Es kann sich
auch in medizinisch und hygienisch unbedenkliche Komponenten
auflösen, so daß es in der Medizin und Landwirtschaft
einsetzbar ist.
Aus pulverisiertem
Glas dieser Art lassen sich beliebig kleine hochporöse
Sinterkörper herstellen, die man mit organischen
Wirkstoffen imprägnieren kann. Wenn sich das Glas in Wasser
oder in Körperflüssigkeit auflöst, gibt es die
Wirkstoffe zeitlich konstant und genau kontrollierbar frei.
Kunststoffe wie Plexiglas fallen wegen ihrer thermodynamischen Eigenschaften (amorpher Aufbau, Glasübergang usw.) ebenfalls in die Kategorie Gläser, obwohl sich ihre chemische Zusammensetzung völlig von der der Silikatgläser unterscheidet. Sie werden daher oft als organisches Glas bezeichnet. Diese Stoffe sind hier nicht Gegenstand der Betrachtung.

Die im allgemeinen Sprachgebrauch bedeutungstragende Eigenschaft von Glas ist die optische Durchsichtigkeit. Die optischen Eigenschaften sind so vielfältig wie die Anzahl der Gläser. Neben klaren Gläsern, die in einem breiten Band für elektomagnetische Wellen durchlässig sind, kann man durch Zugabe von speziellen Materialien zur Schmelze die Durchlässigkeit ändern. Zum Beispiel kann man optisch klare Gläser für infrarotes Licht undurchdringbar machen, die Wärmestrahlung ist blockiert. Die bekannteste Steuerung der Durchlässigkeit ist die Färbung. Es können die verschiedensten Farben erzielt werden. Andererseits gibt es undurchsichtiges Glas, das schon aufgrund seiner Hauptkomponenten oder der Zugabe von Trübungsmitteln opak ist.
Gebrauchsglas hat eine Dichte von ca. 2 500 kg/m3 (Kalk-Natronglas). Die mechanischen Eigenschaften variieren sehr stark. Die Zerbrechlichkeit von Glas ist sprichwörtlich. Die Bruchfestigkeit wird stark von der Qualität der Oberfläche bestimmt. Glas ist weitgehend resistent gegen Chemikalien. Eine Ausnahme ist Flusssäure; sie löst das Siliciumdioxid und wandelt es zu Hexafluorokieselsäure. Bei Raumtemperatur hat Glas einen hohen elektrischen Widerstand, der allerdings mit steigender Temperatur stark abfällt, sofern es sich nicht um Quarzglas (glasartig erstarrtes reines Siliciumdioxid) handelt. Und auch diese Eigenschaften lassen sich schon im Gemenge beeinflussen.
Glas soll mehr als schön sein
Von Ausnahmen abgesehen, diente Glas Jahrtausende bis in die Neuzeit hinein im wesentlichen zur Fertigung von Schmuck und Gefäßen.
Aus den feurigen Flüssen bezaubernde Becher, Vasen und Schalen zu formen war nahezu ausschließlich Ziel der Glasmacher. Glas war ein bevorzugter Werkstoff der
Künstler. Nur am Rande, eher im Schatten der Kunst vollzog sich auch eine technische Entwicklung und Anwendung des Glases.
Dieser Zustand änderte sich ausgangs des 19. Jahrhunderts von Grund auf.
Die aufblühende Industrie verlangte dringend nach mehr und besseren wissentschaftlichen Geräten, Werkstoffen und Halbzeugen, die mitunter völlig neue
chemische und physikaliche Eigenschaften besitzen mußten.
Im Gerätebau, namentlich beim Bau optischer Geräte, nutzte man vor allem die Tatsache, das Glas lichtdurchlässig ist und Licht sowohl
bricht wie auch in seine Farbbestandteile zerlegt.
Es setzet eine ausgedehnte Fertigung optischer Linsen und umfangreicher optischer Systeme ein.
Aus dem Verlangen nach sicherer Naturerkenntnis ergab sich das Bedürfnis nach besseren Abbildungsleistungen der optischen Instrumente. Dafür brauchte
man Gläser mit neuen optischen Eigenschaften.

© biancahoegel.de;
Datum der letzten Änderung: Jena, den: 21.06. 2024