Nukleophile Addition
Die nukleophile Addition (kurz AN) (siehe dazu: Nukleophilie) ist ein Reaktionsmechanismus in der organischen Chemie, bei dem ein Nukleophil (Anion oder Lewis-Base) eine Mehrfachbindung angreift. Das Nukleophil wird der angegriffenen Verbindung hinzugefügt (Addition). Es findet kein Austausch von Atomen oder Atomgruppen statt (vergleiche mit: Substitution).
Edukte
Nukleophil
Als Nukleophile können die verschiedensten Verbindungen eingesetzt werden. Dabei handelt es sich um elektronenreiche, meist freie Elektronenpaare enthaltende, Moleküle oder Anionen (siehe unten: Beispiele).
Mehrfachbindungen
Nukleophile Additionen können an unterschiedlichen Typen von Mehrfachbindungen stattfinden:
- Addition an C=C-Doppelbindungen
- Addition an C≡C-Dreifachbindungen
- Addition an konjugierte C-C-Mehrfachbindungen
- Addition an C-X-Mehrfachbindungen
Reaktionsverlauf
Die Addition des Nukleophils ist normalerweise thermodynamisch kontrolliert; das Nukleophil wird so an die Mehrfachbindung angelagert, dass ein möglichst stabiles Anion resultiert (vergleiche hierzu die Begründung der Markownikow-Regel). Die Stabilisierung erfolgt bei C-X-Mehrfachbindungen durch die Heteroatome selbst, bei substituierten CC-Mehrfachbindungen durch induktive Einflüsse von Substituenten, besonders aber durch Substituenten mit −M-Effekt. Da solche Substituenten gleichzeitig das entferntere C-Atom der Doppelbindung positivieren, ist die Addition an diesem auch kinetisch begünstigt.
Nukleophile Addition an C-C-Mehrfachbindungen
Der erste Schritt bei dieser Reaktion besteht in dem Angriff des Nukleophils unter Bildung eines Carbanions:

Im zweiten Schritt reagiert das Carbanion mit einem Elektronenakzeptor, meist einem Proton:

Die Bildung des Carbanions wird stark begünstigt, wenn die Substituenten dieses durch Mesomerie stabilisieren können. Man spricht dann von einer Michael-Addition, wobei das Nukleophil das Anion einer CH-aciden Verbindung ist.
Nukleophile Addition an C-X-Mehrfachbindungen
CX-Mehrfachbindungen kommen in folgenden Atomgruppen vor:
- Carbonylgruppe
- Thiocarbonylgruppe
- Isocyanatgruppe
- Azomethingruppe
- Cyanogruppe
- Isocyanogruppe
Hier kann ein Nukleophil am Kohlenstoff einer CX-Mehrfachbindung angreifen. Die andere Möglichkeit ist, dass zunächst das elektronenziehende Heteroatom in einem vorgelagerten Gleichgewicht protoniert wird und anschließend das Nukleophil am Kohlenstoff bindet.
Beispiele
Nukleophile Addition an C-C-Mehrfachbindungen
- Addition von Ammoniak oder Aminen
- Addition von Cyanwasserstoff
- Michael-Addition
Nukleophile Addition an C-X-Mehrfachbindungen
Die einzelnen nukleophilen Additionen an C-X-Mehrfachbindungen können anhand des angreifenden Nukleophils in Gruppen eingeteilt werden:
Stickstoff als Nukleophil
- Addition von primären Aminen: Diese Reaktion führt zu einer einem Halbacetal entsprechenden Verbindung (Halbaminal), die in einer Folgereaktion unter Wasserabspaltung in ein Azomethin übergeht.
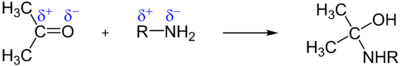
- Addition von sekundären Aminen: Diese Reaktion führt letztendlich zu einem Enamin.
- Addition von Hydrazin
- Addition von Hydroxylamin
- Mannich-Reaktion
Schwefel als Nukleophil
- Mercaptal-Bildung
- Bisulfitaddition
Carbanionischer Kohlenstoff als Nukleophil
- Aldolreaktion
- Benzoin-Addition
- Cyanhydrin-Synthese
- Knoevenagel-Kondensation
- Perkin-Reaktion
- Reformatzki-Reaktion
- Stobbe-Kondensation
- Strecker-Synthese von Aminosäuren
- Wittig-Reaktion


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 04.05. 2025