
Steroid

Steroide (griechisches στερ[ιν]οειδή, von στερεός, stereós: „fest“ (abgeleitet vom Namen des ersten bekannten Steroids, des Cholesterins) und der Endung -oeides „ähnlich“) sind eine Stoffklasse der Lipide (Moleküle mit lipophilen Gruppen, in der Regel wasserunlöslich). Steroide sind Derivate des Kohlenwasserstoffs Steran (Cyclopentanoperhydrophenanthren).
Natürliche Steroide kommen in Tieren, Pflanzen und Pilzen vor; viele werden im glatten endoplasmatischen Retikulum synthetisiert. Ihre biochemischen Aufgaben reichen von Vitaminen und Sexualhormonen (Androgene beim Mann beziehungsweise Estrogene bei der Frau) über Gallensäure und Krötengifte bis zu den herzaktiven Giften von Fingerhut und Oleander.
In Tieren und im menschlichen Organismus stellt Cholesterin das wichtigste Steroid dar; Pflanzen enthalten es dagegen nicht. Aus Cholesterin werden Lipoproteine und Steroidhormone aufgebaut, z.B. die Hormone der Nebennierenrinde (Corticosteroide). Künstliche Derivate des männlichen Sexualhormons Testosteron, die Anabolika, werden als Muskelaufbaupräparate verwendet und sind daher auch als Dopingmittel bekannt.
Struktur
Das Grundgerüst der Steroide ist das Steran. Eine strukturelle Gemeinsamkeit ist der Cyclopentanoperhydrophenanthren-Ring (Ausnahme: Vitamin D). Steroide haben eine starre Molekülgestalt, in der Regel einen relativ hohen Schmelzpunkt und lassen sich gut kristallisieren. Durch die asymmetrischen C-Atome an den Ringverknüpfungen sind zahlreiche Struktur-Isomere möglich, die unterschiedlich gefaltet sind. Nicht alle möglichen Faltungen kommen in der Natur vor. Nach allgemeiner Konvention dient die Position der Methylgruppe am Kohlenstoffatom 10 als Bezugspunkt für die systematische Namensgebung der Isomere: zu der Methylgruppe „quer“ stehende Substitutienten werden mit dem Index α (Alpha) bezeichnet, „längs/parallel“ (trans) stehende mit β (Beta). Bei Gallensäuren z.B. sind die Ringe A und B cis-verknüpft (90° Abwinklung), sie zählen zu den 5β-Androstanen. Steroidhormone sind an dieser Stelle dagegen trans-verknüpft (5α-Androstane). Nebengruppen werden abgekürzt ((z.B. „-ol“ = Alkoholgruppe). Die Position von Doppelbindungen wird mit einem Δ (Delta) angegeben. Der systematische Name von Cholesterin ist z.B. Cholest-Δ5-en-3β-ol.
Biosynthese der Steroidhormone
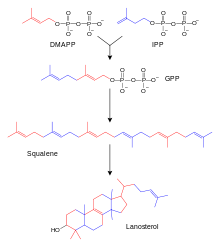
Die Biosynthese der Steroide gleicht zunächst in Grundzügen der Biosynthese der Terpene. Ein wichtiger Zwischenschritt führt zu Squalen, einem Triterpen. Lanosterol entsteht durch mehrere zyklische Verknüpfungen. Dieses Steroid mit Sterangrundgerüst liefert unter Abspaltung dreier Methylgruppen, Hydrierung und Isomerisierung Cholesterin. Über drei verschiedene Wege entstehen aus Cholesterin Aldosteron, Testosteron und Cortisol. Dies geschieht in der Nebennierenrinde und in den männlichen und weiblichen Gonaden (Hoden und Ovar). Im Ovar wird zunächst auch Testosteron (männliches Geschlechtshormon) produziert, das dann mit einer Aromatase (Enzym, das den Ring A des Steroidgerüstes zu einem Benzolring dehydriert) zu Estradiol umgebaut wird. Die Enzyme, welche die einzelnen Schritte vom Cholesterin zu den Steroidhormonen katalysieren, können durch Gendefekte gestört sein. Relativ häufig ist der 21-Hydroxylase-Mangel. Dieser führt zu einer Überproduktion von Geschlechtshormonen, da der Weg zum Cortisol und Aldosteron gestört ist. Die Krankheit nennt sich Adrenogenitales Syndrom.
Abbau
Im Menschen werden die Steroide in der Leber durch Hydroxylierung und Konjugation mit Glycin oder Taurin wasserlöslich gemacht und als Gallensäuren über die Galle ins Duodenum (vorderer Teil des Dünndarms) ausgeschieden.
Einteilung
- Sterine (Sterole) (beispielsweise Cholesterin (Cholesterol), Ergosterin (Ergosterol))
- Gallensäuren (beispielsweise Cholsäure)
- Steroidhormone
- Glucocorticoide (beispielsweise Cortison)
- Mineralocorticoide (beispielsweise Aldosteron)
- Estrogene (beispielsweise Estron, Estradiol)
- Gestagene (beispielsweise Progesteron)
- Androgene (beispielsweise Testosteron, Androsteron)
- Insektenhormone (beispielsweise Ecdyson)
- herzwirksame Steroide (Aglykone
der Herzglykoside)
- Cardenolide (beispielsweise Digoxigenin, Digitoxigenin, Gitoxigenin, Strophanthidin)
- Bufadienolide (beispielsweise Cillarenin, Hellebrigenin, Uzarigenin)
- Sapogenine (beispielsweise Digitogenin, Diosgenin)
- Steroidalkaloide (beispielsweise Solanidin, Tomatidin)


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 14.10. 2020