Manganate
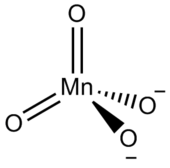
Manganat-Ion

Grüne Farbe
des Manganat-Ions
Manganate oder Manganate(VI) sind chemische Verbindungen des Mangans. Es handelt sich um Salze mit dem zweifach negativ geladenen MnO42−-Anion, die sich von der in freier Form unbeständigen Mangansäure (H2MnO4) ableiten. Die Manganat-Ionen sind nur in stark basischer Lösung stabil und paramagnetisch. Lösungen mit Manganat-Ionen erscheinen grün.
Die technische Herstellung erfolgt unter anderem aus Braunstein (MnO2) im stark Alkalischen unter Luftzufuhr (von Oxidationsstufe IV nach VI):
Eine Labordarstellung gelingt durch Oxidationsschmelze aus Mn(II):
Verbindungen
Literatur
- N. N. Greenwood und A. Earnshaw: Chemie der Elemente, 1. Auflage, VCH, Weinheim 1988, ISBN 3-527-26169-9.
- Jander/Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie, 12. Auflage, S. Hirzel Verlag, Stuttgart 1983, ISBN 3-7776-0379-1.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 12.02. 2022