
Sulfonsäureamide
| Sulfonsäureamide |
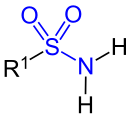 Primäres Sulfonsäureamid, R1 ist ein Organyl-Rest (Alkyl-Reste, Aryl-Reste, Arylalkyl-Reste etc.). |
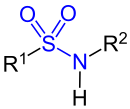 Sekundäres Sulfonsäureamid, R1 und R2 sind Organyl-Reste (Alkyl-Reste, Aryl-Reste, Arylalkyl-Reste etc.). |
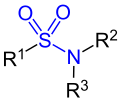 Tertiäres Sulfonsäureamid, R1 bis R3 sind Organyl-Reste (Alkyl-Reste, Aryl-Reste, Arylalkyl-Reste etc.). |
Sulfonsäureamide sind eine Stoffgruppe organisch-chemischer Schwefelverbindungen die als Amide der Sulfonsäuren beschrieben werden können. Sie enthalten eine Sulfonamidgruppe, die exakter als Sulfonsäureamidgruppe bezeichnet wird.
Sulfonsäureamide sind polare Feststoffe, ihr einfachster Vertreter ist Methansulfonsäureamid.
Bezeichnung als funktionelle Gruppe in der systematischen Namensgebung: Sulfamoyl-, -sulfonamid, -sulfamid
Herstellung
Bei der Reaktion von Sulfonsäurechloriden mit Ammoniak, primären Aminen oder sekundären Aminen entstehen Sulfonsäureamide.[1]
Bedeutung
Die wichtigsten Vertreter dieser Stoffgruppe sind die antibiotisch wirksamen Sulfonamide, die als Arzneistoffe praktische Bedeutung besitzen.[2]
Nur noch chemiehistorische Bedeutung hat die Hinsberg-Trennung, eine analytische Methode zur Trennung primärer, sekundärer und tertiärer Amine. Dabei reagieren tertiäre Amine nicht mit Benzolsulfonsäurechlorid. Die Sulfonsäureamide primärer Amine lassen sich von den Sulfonsäureamiden sekundärer Amine abtrennen, da erstere ein acides Wasserstoffatom am Stickstoffatom enthalten, das mit Natronlauge deprotoniert werden kann und somit wasserlöslich wird.[3]
Literatur
- Eintrag zu sulfonamides. In: IUPAC (Hrsg.):
Compendium of Chemical Terminology. The “Gold Book”.
doi:
 10.1351/goldbook.S06114.
10.1351/goldbook.S06114.
Einzelnachweise
- ↑ Siegfried Hauptmann: Organische Chemie, 2. durchgesehene Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, S. 485–486, ISBN 3-342-00280-.
- ↑ Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 5: Pl–S. 8. neubearbeitete und erweiterte Auflage. Franckh’sche Verlagshandlung, Stuttgart 1987, ISBN 3-440-04515-3, S. 4051–4052.
- ↑ Brockhaus ABC Chemie, VEB F. A. Brockhaus Verlag Leipzig 1965, S. 542.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 12.12. 2024