
Glaselektrode
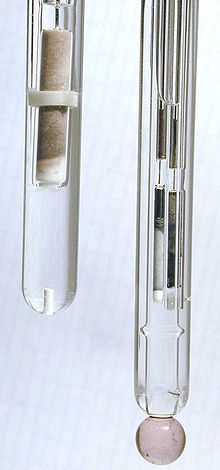
Die Glaselektrode ist die häufigste Variante einer pH-Elektrode und wird zur Messung des pH-Wertes, der Wasserstoffionenaktivität, eingesetzt.
Sie ist in der täglichen Laborpraxis geeigneter als die Wasserstoffelektrode. Die Glaselektrode muss allerdings mit Lösungen bekannten pH-Wertes kalibriert werden. Das sich an einer Glaselektrode einstellende Potential ist abhängig von der Wasserstoffionenaktivität und folgt nicht der Nernst-Gleichung.
Prinzipiell sind zur pH-Messung zwei Elektroden notwendig, die Bezugselektrode und die Glaselektrode selbst. Meistens wird jedoch eine Bauform gewählt, bei der beide Elektroden in einer sogenannten Einstabmesskette vereint werden.
Die kombinierte Glaselektrode
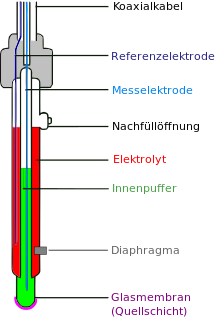
Diese Einstabmesskette ist aus einem inneren Rohr und einem äußeren Mantel aufgebaut. Der äußere Mantel dient als Referenzelektrode (Silber-Silberchlorid-Elektrode) und besteht aus einem Silberdraht, Silberchlorid und einer Elektrolytlösung (meist Kaliumchlorid). Auch im inneren Rohr befinden sich Silberdraht, Silberchlorid und Kaliumchloridlösung, die zusätzlich noch einen Puffer (Phosphatpuffer) enthält. Das innere Rohr ist mit der Glasmembran mit der zu messenden Lösung verbunden, der äußere Mantel wiederum mit einem Diaphragma. Daraus ergibt sich die elektrochemische Reihe:
Ag | AgCl | KCl-Lösung || Glasmembran || Messlösung || Diaphragma || KCl-Lösung | AgCl | Ag
Vereinfacht entsteht das Potential der Glaselektrode dabei wie folgt:
Die Referenzelektrode steht über ein Diaphragma (meist Platinschwamm oder poröse Keramik) in elektrischem Kontakt mit der Messlösung, wobei das Diaphragma Stoffaustausch mit der Lösung aber weitgehend unterbindet, um das Potential der Referenzelektrode nicht durch Fremdionen zu verändern. In dem Messstab befindet sich die Messelektrode in einer auf pH 7 eingestellte, gepufferte Kaliumchloridlösung. Diese steht durch eine sehr dünne Glasmembran (≈ 50 µm) in leitender Verbindung mit der Messlösung, an der das zur pH-Messung verwendete Potential entsteht. Die in der Glasmembran befindlichen Natrium- und Lithiumionen sind relativ frei beweglich, für Wasserstoffionen ist die Membran aber undurchlässig. Dennoch können die Wasserstoffionen Gitterplätze an den Sauerstoffanionen der unterkühlten Silikatschmelze (siehe Chemischer Aufbau von Glas) einnehmen, da diese bei Kontakt mit der wässrigen Lösung an der Oberfläche beginnt aufzuquellen. Ein niedriger pH-Wert hat zur Folge, dass die Wasserstoffionen die Gitterplätze bevölkern und Natrium- und Lithiumionen in die Membran „zurückdrängen“. Da diese in der Membran frei beweglich sind, werden sie tendenziell auf die Innenseite der Membran verschoben, die gemessene Potentialdifferenz entsteht. Bei einem hohen pH überwiegt die Wasserstoffionenkonzentration im Inneren des Messstabes, der beschriebene Prozess läuft in anderer Richtung ab, das Potential entsteht mit anderem Vorzeichen.
Verwendung und Einsatzgebiete
Die Elektrode darf niemals trocken oder in destilliertem Wasser längere Zeit gelagert werden, sondern sollte in einer 3 molaren wässriger KCl-Lösung gelagert werden. Einsatzgebiete sind:
- Messung des pH-Wertes im Labor
- Online-Messung des pH-Wertes im industriellen Prozess, z.B. in der Chemie, Biotechnologie, Wasser- und Abwasserbehandlung, Lebensmittel- und Getränkeindustrie etc.
- Durchführung von Säure-Base-Titrationen
- pH-Wert-Bestimmung in Aquarien
Siehe auch


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 08.11. 2023