
Volumenarbeit
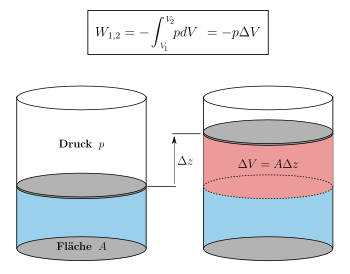
Die Volumenarbeit oder Volumenänderungsarbeit ist die an einem
geschlossenen
System zu leistende Arbeit
,
um ein Volumen
auf das Volumen
zu verändern:
- bei der Volumenverkleinerung
durch Kompression wird Kompressionsarbeit geleistet, d.h. dem System zugeführt (in der Abbildung ist dies die Arbeit, die der Kolben an dem im Zylinder enthaltenen Gas verrichtet):
- bei der Volumenvergrößerung
durch Expansion wird Arbeit – d.h. Energie – frei, d.h. vom System abgegeben:
Die Formel für die Volumenarbeit lautet:
.
Hierbei ist
die Kraft, die
längs eines Weges
wirkt; dieser wird in Expansionsrichtung positiv gezählt (in der
Abbildung entgegen der gezeigten Kompressionskraft
).
Das Minuszeichen in der Formel ist eine Konvention;
so wird erreicht, dass dem System zugeführte Arbeit wie oben beschrieben positiv
ist, freiwerdende Energie dagegen ein negatives Vorzeichen erhält. Bei der
dargestellten Kompression hat der zurückgelegte Weg ein negatives Vorzeichen
welches durch das zusätzliche Minuszeichen in der Formel für die Volumenarbeit
kompensiert wird.
Reibungsloser Vorgang
Die reibungsfrei
und quasistatisch zugeführte
Arbeit ist in dem dargestellten Zylinder mit dem Querschnitt
wegen
(Reibungsfreiheit):
mit
: Druck
: Volumenänderung.
Diese Zustandsänderung
verläuft im p-V-Diagramm
vom Punkt 1 zum Punkt 2, bei der dargestellten Kompression also in
negativer Volumenrichtung
daher hätte die Kompressionsarbeit ohne das Minuszeichen in der Formel ein
negatives Vorzeichen.
Der Integralwert, der der Fläche unter dem Zustandsverlauf entspricht, lässt sich berechnen, wenn die Funktion p = f(V) bekannt ist (s.u.).
Reibungsbehafteter Vorgang
Im realen Fall, wenn zwischen dem Kolben und dem Zylinder eine Reibungskraft wirkt, muss
beim Komprimieren zusätzlich zur Volumenänderungsarbeit die Reibungsarbeit
aufgebracht werden. Diese erhöht die innere
Energie des Systems und damit den Druck gegenüber dem reibungsfreien Vorgang
(wenn sie nicht durch Kühlung
als Wärme
nach außen abgeführt wird):
Im p-V-Diagramm verläuft die Zustandsänderung nun vom Punkt 1 zum Punkt 2’. Das heißt, dass auch die Volumenänderungsarbeit, die der Fläche unter dem Verlauf entspricht, größer wird, ohne dass darin die Reibungsarbeit selbst enthalten ist:
Die von außen aufzubringende Arbeit ist also die Summe aus der nunmehr größeren Volumenänderungsarbeit und der Reibungsarbeit:
Berechnungsbeispiel
Angenommen sei die isotherme
Verdichtung eines idealen
Gases
Dann lässt sich durch Einsetzen der thermischen Zustandsgleichung idealer Gase:
mit
- n die Stoffmenge
- R die allgemeine Gaskonstante
- T die absolute Temperatur
das Integral für die Volumenarbeit lösen:
Anhand dieser Gleichung sieht man, dass bei der Expansion eines idealen Gases die Volumenarbeit negativ ist, also Energie frei wird; dies folgt aus dem Logarithmus, der für Zahlen kleiner eins negativ und für Zahlen größer eins positiv ist:
Statt n·R kann man oben auch m·Rs einsetzen:
wobei
- m die Masse des Stoffes und
- Rs seine spezifische Gaskonstante ist.
Wird die Kompression in einem offenen System mit dem Außendruck
durchgeführt, muss an tatsächlicher Arbeit
aufgebracht werden, da der Außendruck mit der Fläche multipliziert ebenfalls eine Kraft ergibt. Ist der Außendruck höher als der Innendruck des zu komprimierenden Volumens wird dabei Energie gewonnen, ist er geringer muss dabei Arbeit geleistet werden.
Siehe auch


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 17.02. 2023