
Occludin
| Occludin | ||
|---|---|---|
| ||
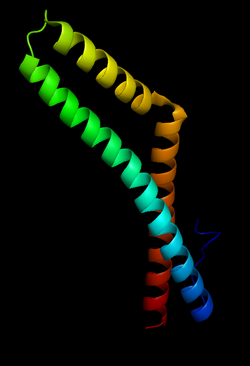
| Struktur des C-Terminus von Occludin PDB
| ||
| ||
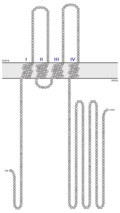
| Transmembrandomänen von menschlichem Occludin | ||
|
Vorhandene Strukturdaten: 1XAW | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 59,144 kDa / 522 Aminosäuren | |
| Bezeichner | ||
| Gen-Name | | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | | |
Occludin (von lateinisch occludere, deutsch: verschließen) ist ein Protein, das zusammen mit den Proteinen der Claudin-Familie an der Bildung der Tight junctions beteiligt ist, welche in Epithelzellen vorkommen. Tight junctions verschließen in den Epithelien die Zellzwischenräume und schützen den Körper sowohl vor Austrocknung als auch vor äußeren Einflüssen (z. B. vor dem sauren Inhalt des Magens mit pH zwischen 1 und 2). Mutationen im OCLN-Gen sind die Ursache für das seltene Aicardi-Goutières-Syndrom.[1]
Entdeckung
Occludin wurde 1993 erstmals von der Arbeitsgruppe um Mikio Furuse und Shoichiro Tsukita beschrieben. Sie fraktionierten Extrakte aus Hühnerleber und fanden ein Protein mit einer Molaren Masse von 55,9 kDa, das aus 504 Aminosäuren bestand. Der Hydrophilie-Plot erinnerte die Wissenschaftler stark an das Protein Connexin (ebenfalls vier Transmembran-Domänen nahe dem N-Terminus).[2]
Aufbau
Occludin ist ein Transmembranprotein mit vier Transmembran-Domänen, weshalb es in fünf verschiedene Domänen aufgeteilt werden kann (jeweils unterbrochen von einer Transmembran-Domäne), welche A-E genannt werden.Dadurch besitzt das Protein zwei extrazelluläre Schleifen, welche beide etwa gleich groß (jeweils 45 Aminosäuren) sind, eine kurze intrazelluläre Schleife, welche die beiden extrazelluläre Schleifen verbindet, sowie zwei lange Ketten am N- und C-Terminus. Die beiden extrazellulären Schleifen sind notwendig, um die Funktion (Zell-Zell-Verbindung) aufrechtzuerhalten und eine davon scheint in der Lokalisation von Occludin in den tight junctions eine Rolle zu spielen.[1] Die E-Domäne (nahe dem C-Terminus; siehe Abbildung) ist im Cytoplasma lokalisiert und ist notwendig, um das Protein ZO-1 zu binden. Tight junctions können nach dem Einbau von mutiertem Occludin durchlässiger werden.[3] Knockout-Modelle zeigen jedoch, dass die Barrierefunktion der Tight junctions ohne Occludin bestehen bleibt.[4] Andererseits beeinflusst Occludin Signalwege, die das Überleben von Darmepithelzellen fördern.[5]
Bis jetzt (2005) wurden fünf verschiedene Typen von Occludin gefunden (Typ I bis IV)[6] sowie Occludin 1B[7] welche aus unterschiedlichem Splicing der mRNA hervorgehen. Dies könnte darauf hinweisen, dass mehrere Proteine mit ähnlichen Eigenschaften (wie bei den Claudinen) eine Occludin Protein-Familie bilden könnten.
Interaktionen
Die ersten Interaktionspartner von Occludin wurden mit ZO-1 und ZO-2 bestimmt. Später wurde noch das Protein ZO-3 identifiziert, das ebenfalls eine Interaktion mit Occludin eingeht. Es wird vermutet, dass ZO-1 direkt Occludin bindet und dieses mit dem Aktin-Cytoskelett verbindet. Es wurden noch Interaktionen von Occludin mit JAM, VAP-33, JEAP und CLMP gefunden. Außerdem wird Occludin sehr wahrscheinlich von der Proteinkinase C (PKC) phosphoryliert, was dann die Verteilung und Funktion des Proteins in der Zelle verändert (die phosphorylierte Form scheint die aktive Form zu sein). Weiterhin könnten Ras-ähnliche G-Proteine wie RhoA und Rac-1 bei der Regulation des Occludins eine Rolle spielen, sowie auch Cytokine in dem Regulationsprozess eine Rolle spielen.[1]
Quellen
- ↑ Hochspringen nach: a b c Gemma J. Feldmana,
James M. Mullinb, Michael P. Ryan: Occludin: Structure, function and regulation. In: Adv Drug Deliv Rev. 57(6), 25. Apr 2005, S. 883–917.
 PMID 15820558.
PMID 15820558.
- ↑ M. Furuse, T. Hirase, M. Itoh, A. Nagafuchi, S. Yonemura, S.Tsukita, S. Tsukita: Occludin a novel integral membrane protein
localizing at tight junctions. In: J Cell Biol. 123(6 Pt 2), Dezember 1993, S. 1777–1788.
 PMID 8276896.
PMID 8276896.
- ↑ S. D. Bamforth, U. Kniesel, H. Wolburg, B. Engelhardt, W. Risau: A dominant mutant of occludin disrupts tight junction structure
and function. In: J Cell Sci. 112 ( Pt 12), Jun 1999, S. 1879–1888.
doi:
 10.1242/jcs.112.12.1879.
10.1242/jcs.112.12.1879.
 PMID 10341207.
PMID 10341207.
- ↑ Jörg-Dieter Schulzke, Alfred H. Gitter, Joachim Mankertz, Stefanie Spiegel, Ursula Seidler, Salah Amasheh, Mitinori Saitou,
Shoichiro Tsukita, Michael Fromm: Epithelial transport and barrier function in occludin-deficient mice. In: Biochim Biophys Acta. 1669(1), 15. Mai 2005, S. 34–42.
doi:
 10.1016/j.bbamem.2005.01.008.
10.1016/j.bbamem.2005.01.008.
 PMID 15842997.
PMID 15842997.
- ↑ W.-T. Kuo, M. A. Odenwald, J. R. Turner, L. Zuo: Tight junction proteins occludin and ZO-1 as regulators of epithelial proliferation and
survival. In: Ann N Y Acad Sci. 1514(1), Aug 2022, S. 21–33.
doi:
 10.1111/nyas.14798.
10.1111/nyas.14798.
 PMID 35580994.
PMID 35580994.
- ↑ J. Mankertz, J. S. Waller, B. Hillenbrand, S. Tavalali, P. Florian, T. Schoneberg, M. Fromm, J. D. Schulzke: Gene expression of
the tight junction protein occludin includes differential splicing and alternative promoter usage. In: Biochem Biophys Res Commun. 298(5), 15. Nov 2002, S. 657–666.
 PMID 12419305.
PMID 12419305.
- ↑ Z. Muresan, D. L. Paul, D. A. Goodenough: Occludin 1B, a variant of the tight junction protein occludin. In: Mol Biol Cell.
11(2), Feb 2000, S. 627–634.
 PMID 10679019.
PMID 10679019.


© biancahoegel.de
Datum der letzten Änderung: Jena, den: 07.03. 2026